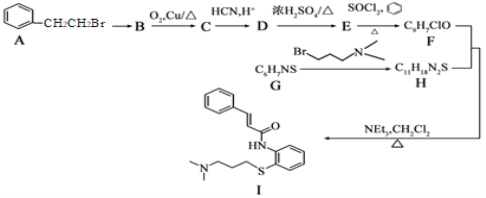
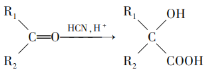
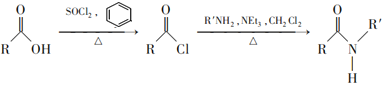
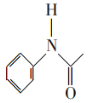
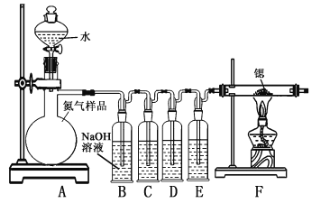
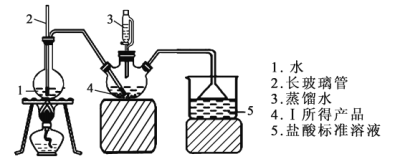
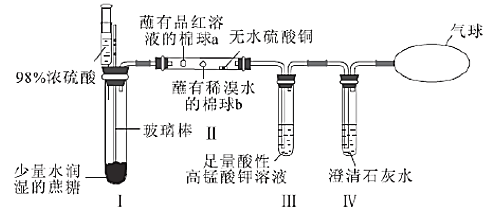
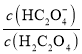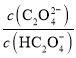【题目】某同学设计了蔗糖与浓硫酸反应的改进装置,并对气体产物进行检验,实验装置如图所示。下列结论中正确的是( )
选项 | 现象 | 结论 |
A. | Ⅰ中注入浓硫酸后,可观察到试管中白色固体变为黑色 | 体现了浓硫酸的吸水性 |
B. | Ⅱ中观察到棉球a、b都褪色 | 均体现了SO2的漂白性 |
C. | Ⅱ中无水硫酸铜变蓝 | 说明反应产物中有H2O |
D. | Ⅲ中溶液颜色变浅,Ⅳ中澄清石灰水变浑浊 | 说明有CO2产生 |
A.AB.BC.CD.D
【题目】三氧化二钴(Co2O3)主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。以含钴废料(主要成分为Co2O3,含有少量MnO2、NiO、Fe3O4)为原料制备Co2O3的流程如下图所示:

已知:
Ⅰ.“酸浸”后的浸出液中含的阳离子有H+、Co2+、Fe3+、Ni2+等。
Ⅱ.部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
沉淀物 | Fe(OH)3 | Co(OH)2 | Ni(OH)2 |
完全沉淀时的pH | 3.7 | 9.0 | 9.2 |
回答下列问题:
(1)“酸浸”含钴废料的温度不宜过高,原因是_____________。
(2) “酸浸”时发生的主要反应是___________________(写离子方程式)。
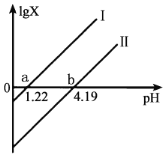
(3)某萃取剂对金属离子的萃取率与溶液pH的关系如图所示:
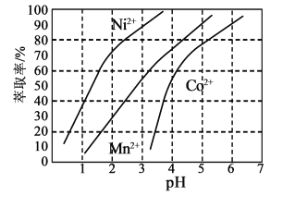
使用该萃取剂时应控制的pH约为____________,理由是_____________。
(4)写出高温煅烧时发生的化学反应方程式___________。
(5)操作1得到的副产品是__________(填名称);
已知该物质的溶液加热到100℃时会变质,该物质的溶解度见下表:
湿度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ |
溶解度 | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 88.0 |
操作1是________(填字母)。
a.蒸发结晶 b.降温结晶 c.减压蒸发结晶
(6)有机相提取的Ni2+再生时可用于制备镍氢电池,该电池充电时的总反应为Ni(OH)2+M=NiOOH+MH,则放电时负极的电极反应式为_________________。
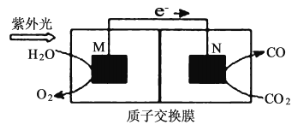
【题目】浙江师范大学的研究团队研究获得了一类具有高活性和选择性的钙钛矿光催化剂(![]() ),这一成果发表在2020年1月Chem. Mater.上。带有负电荷的CsPbBr3将带正电的
),这一成果发表在2020年1月Chem. Mater.上。带有负电荷的CsPbBr3将带正电的![]() 固定在其表面,用于可见光驱动CO2还原。
固定在其表面,用于可见光驱动CO2还原。

(1)写出Ni基态原子的价电子排布图(轨道表达式)___________________。
(2)C、N、O、Cs、Pb元素第一电离能由大到小的顺序是____________________。
(3)![]() 是二价阳离子,该离子中氮原子的杂化类型为_________,该离子结构中含有_________(填字母)。
是二价阳离子,该离子中氮原子的杂化类型为_________,该离子结构中含有_________(填字母)。
a.离子键 b.配位键 C.π键 d.氢键
(4)某些氧化物的熔点数据如下表所示:
氧化物 | CO2 | Cs2O | PbO |
熔点/℃ | -56.6 | 490 | 888 |
解释表中氧化物之间熔点差异的原因:______________________________。
(5)氮化镓是一种半导体材料。晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。
①与同一个Ga原子相连的N原子构成的空间构型为__________;
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如图,则2、3、4原子的分数坐标不可能的是(________________)
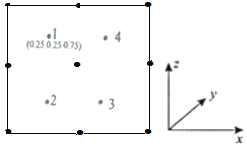
a.(0.75,0.25,0.25) b.(0.25,0.75,0.75)
c.(0.25,0.75,0.25) d.(0.75,0.75,0.75)
③ GaN晶体中N和N的原子核间距为a pm,GaN摩尔质量为![]() ,阿伏加德罗常数的值为NA,则GaN晶体的密度为___________
,阿伏加德罗常数的值为NA,则GaN晶体的密度为___________![]() (
(![]() )。
)。