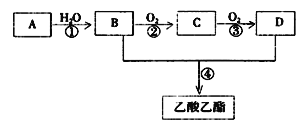
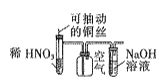
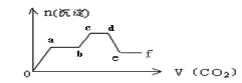
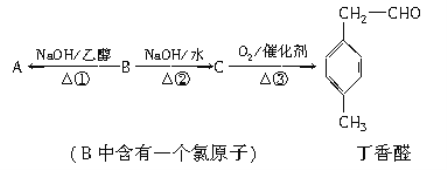
【题目】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
二 |
|
| ||||||
三 |
|
|
|
|
|
| ||
四 |
(1)9种元素中,化学性质最不活泼的是______,原子结构示意图为____________。
(2)这些元素中,最高价氧化物的水化物中碱性最强的碱是__________,写出元素![]() 的单质与其反应的离子方程式:___________________________________。
的单质与其反应的离子方程式:___________________________________。
(3)最高价氧化物是两性氧化物的元素是______ ,写出它的氧化物与NaOH溶液反应的化学反应方程式: ____________________________________ 。
(4)用电子式表示元素![]() 和
和![]() 组成的化合物的形成过程 _____________________________,该化合物属于 ______ (填“共价”或“离子”
组成的化合物的形成过程 _____________________________,该化合物属于 ______ (填“共价”或“离子”![]() 化合物。
化合物。
【题目】描述弱电解质电离情况可以用电离度和电离平衡常数表示,表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),表2是常温下几种难(微)溶物的溶度积常数(Ksp)。
表1
酸或碱 | 电离平衡常数(Ka或Kb) |
CH3COOH | 1.8×10-5 |
HNO2 | 4.6×10-4 |
HCN | 5×10-10 |
HClO | 3×10-8 |
NH3·H2O | 1.8×10-5 |
表2
难(微)溶物 | 溶度积常数(Ksp) |
BaSO4 | 1×10-10 |
BaCO3 | 2.6×10-9 |
CaSO4 | 7×10-5 |
CaCO3 | 5×10-9 |
请回答下列问题:
(1)表1所给的四种酸中,酸性最弱的是________(用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是________(填字母序号)。
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈________(选填“酸性”、“中性”或“碱性”),该溶液中存在的各离子浓度大小关系是_____________________________。
(3)物质的量之比为1∶1的NaCN和HCN的混合溶液,其pH >7,该溶液中离子浓度从大到小的排列为________________________。
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度不小于0.01 mol·L-1,则溶液中CO32-物质的量浓度应 ≥ ______________。