现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 第三周期元素的简单离子中半径最小 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是____________(用元素符号表示)元素Z的离子结构示意图为_________________。
(2)金属镁可以在元素X的最高价氧化物中燃烧的化学方程式:______________
(3)元素Y的与氢元素形成一种离子YH4+,写出其电子式_________________。
(4)写出Z元素最高价氧化物与NaOH溶液反应的离子方程式:_______________。
(5)元素X与元素Y相比,非金属性较强的是______(用元素符号表示)。下列表述中证明这一事实的是____________。
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物水化物的酸性比X的最高价氧化物水化物的酸性强
c.X与Y形成的化合物中X元素呈正价态
(6)探寻物质的性质差异性是学习的重要方法之一。X、Y、Z三种元素的单质中化学性质明显不同于其他两种单质是___________(用元素符号表示),理由_________。
现有几种元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 失去一个电子后,形成Ne原子电子层结构 |
X | 短周期非金属,其最外层电子数是次外层电子数的一半 |
Y | 其单质之一是空气中主要成分,最常见的助燃剂 |
Z | 形成双原子单质分子,黄绿色气体 |
(1)工业制备X单质反应的化学方程式_______________________________;
(2)画出T的离子结构示意图__________;
(3)写出实验室利用浓盐酸和二氧化锰制取单质Z的离子方程式______________________;
(4)由T和Y两种元素组成的一种阴阳离子个数比为1:2的过氧化物,其电子式为___________。写出该物质的一种用途__________________________________
(5)T、Z的最高价氧化物对应的水化物相互反应的离子方程式为___________________。

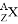 ,它的氯化物XCl2 1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,求:
,它的氯化物XCl2 1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,求: