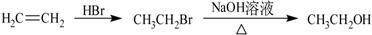设NA阿伏伽德罗常数的值。己知反应
(1)CH4(g)+2O2(g)═CO2(g)+2H2O(l) △H1=a kJ/mol
(2)CH4(g)+2O2(g)═CO2(g)+2H2O(g) △H2=b kJ/mol,其它数据如表:
化学键 | C═O | O═O | C-H | O-H |
键能kJ·mol-1 | 798 | x | 413 | 463 |
下列说法正确的是
A.上表中 x=(1796+b)/2
B.H2O(g)═H2O(l) △S<0,△H═(a-b )kJ/mol
C.当有4NA个C-H键断裂时,该反应放出热量一定为a kJ
D.利用反应(1)设计的原电池电解精炼铜时,当负极输出0.2NA个电子时,电解槽的阳极质量一定减轻6.4g
三氯化磷(PCl3)是一种用于有机合成的重要催化剂。实验室常用红磷与干燥的Cl2制取PCl3,装置如图所示。
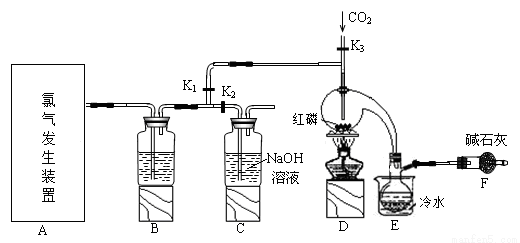
已知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇O2会生成POCl3(三氯 氧磷), POCl3溶于PCl3,PCl3遇水会强烈水解生成H3PO3和HCl。PCl3、POCl3的熔沸点见下表。
物质 | 熔点/℃ | 沸点/℃ |
PCl3 | -112 | 75.5 |
POCl3 | 2 | 105.3 |
请答下面问题:
(1)玻璃管之间的连接需要用到胶皮管,连接的方法是:先把 ,然后稍稍用力即可把玻璃管插入橡皮管。
(2)B中所盛试剂是 ,F中碱石灰的作用是 。
(3)实验时,检查装置气密性后,向D装置的曲颈瓶中加入红磷,打开K3通入干燥的CO2,一段时间后,关闭K3,加热曲颈瓶至上部有黄色升华物出现时通入氯气,反应立即进行。通干燥CO2的作用是 ,C装置中的K1、 K2的设计也出于类似的目的,为了达到这—实验目的,实验时与K1、K2有关的操作是 。
(4)实验制得的粗产品中常含有POCl3、PCl5等。加入红磷加热除去PCl5后,通过 (填实验操作名称),即可得到较纯净的PCl3。
(5)通过下面方法可测定产品中PCl3的质量分数:
①迅速称取1.00g产品,加水反应后配成250mL溶液:
②取以上溶液25.00mL,向其中加入10.00mL0.1000mol/L碘水(足量),充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000 mol/L的Na2S2O3溶液滴定;
④重复②、③操作,平均消耗0.1000 mol/L Na2S2O3溶液8.00mL.
己知:H3PO3+I2+H2O=H3PO4+2HI,I2+2Na2S2O3=2NaI+Na2S4O6,根据上述数据,假设测定过程中没有其他反应,该产品中PCl3的质量分数为 。
 2
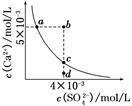
2 SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是

 2NH3(g)。
2NH3(g)。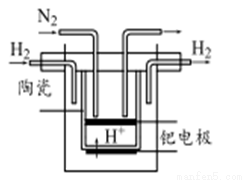
 4NH3(g)+3O2(g),则其反应热△H= 。(已知:N2(g)+3H2(g)
4NH3(g)+3O2(g),则其反应热△H= 。(已知:N2(g)+3H2(g) 


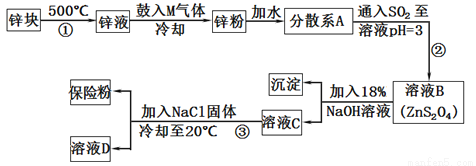
 )的合成路线(无机原料任选)。合成路线流程图示例如下:
)的合成路线(无机原料任选)。合成路线流程图示例如下: