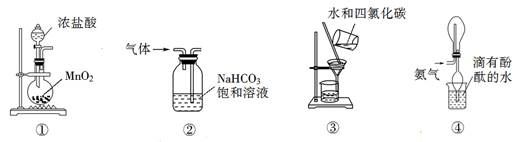
题目内容
某温度下,将2molSO2和1molO2置于10L密闭容器中发生反应:2SO2(g)+O2(g)  2
2 SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是

A.由图甲推断,B点SO2的平衡浓度为0.3 mol·L-1
B.由图甲推断,A点对应温度下该反应的平衡常数为800(L·mol-1)
C.达平衡后,若增大容器容积,则反应速率变化图像可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
练习册系列答案
相关题目


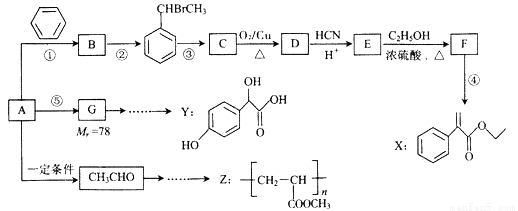

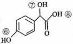 )的说法正确的是 。(双选)
)的说法正确的是 。(双选)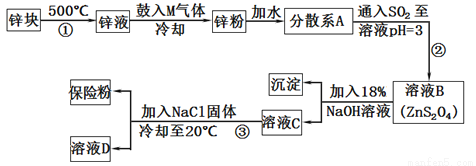

 的原理如图2所示,阴极反应式为 。假设降解前两极溶液质量相等,当电路中有2mol电子通过时,此时两极溶液质量的差值为 g。
的原理如图2所示,阴极反应式为 。假设降解前两极溶液质量相等,当电路中有2mol电子通过时,此时两极溶液质量的差值为 g。
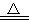 2MgO+Si
2MgO+Si