0 174972 174980 174986 174990 174996 174998 175002 175008 175010 175016 175022 175026 175028 175032 175038 175040 175046 175050 175052 175056 175058 175062 175064 175066 175067 175068 175070 175071 175072 175074 175076 175080 175082 175086 175088 175092 175098 175100 175106 175110 175112 175116 175122 175128 175130 175136 175140 175142 175148 175152 175158 175166 203614


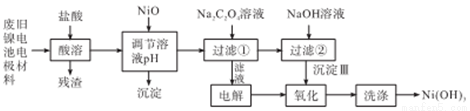

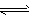 2NH3,该过程中还原反应的方程式为________________。
2NH3,该过程中还原反应的方程式为________________。

 。
。 的合成路线流程图(注明反应条件):合成路线流程图示例如下:
的合成路线流程图(注明反应条件):合成路线流程图示例如下: ________
________ 。
。
 ,列式并计算出结果)
,列式并计算出结果)

