下列实验操作能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 检验Fe(NO3)2样品已被氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 |
B | 提取碘水中碘 | 将碘水倒入分液漏斗,加入适量乙醇,振荡后静置 |
C | 验证Mg(OH)2沉淀可以转化为 Fe(OH)3沉淀 | 向 2 mL1mol·L-1NaOH 溶液中加入2 ~3 滴 lmol·L-1MgCl2溶液,生成白色沉淀,再加入2~3滴lmol·L-1FeCl3溶液 |
D | 比较碳和硅的非金属性强弱 | 向饱和的Na2SiO3溶液中通人CO2 |
“一器多用”可实现多方面的化学实验探究,某课外活动小组学生利用图15所示的仪器组合(省略夹持和净化装置)来完成下列实验,回答下列问题:
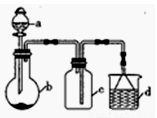
(1)仪器a的名称为______________,仪器a在使用前要________________。
(2)该装置可用于某些气体的制取、收集及尾气处理裝置,下表中3个实验的设计方案合理的是_________________(填序号)
选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 稀硝酸 | Cu | NO | H2O |
B | 稀H2SO4 | CaCO3 | CO2 | NaOH溶液 |
C | 浓氨水 | NaOH固体 | NH3 | H2O |
(3)氨气和氯气接触时会产生白烟,请写出相应的化学方程式:_______________________。
(4)上述装置若a中的物质为浓硫酸,b中的物质为Cu片,在加热条件下也可制取SO2。
①下列装置可用于SO2尾气处理的是(夹持仪器已略去)_____________(填序号)。
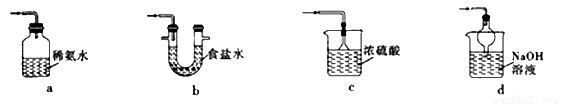
用Fe2(SO4)3溶液也可吸收多余的SO2气体.写出SO2与Fe2(SO4)3溶液反应的离子方程式:_______________________。
②某小组用反应产生的CuSO4溶液来制取胆矾,测定所得胆矾(CuSO4·xH2O)中结晶水x的值,各次 称量的数据如下表:
称量 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
质量(g) | m1=5.4 | m2=8.2 | m3=7.4 | m4=7.2 | m5=7.2 |
则胆矾应放在____________(填仪器名称)中加热;必须要进行恒重操作的原因是__________________;CuSO4·xH2O中的x=___________(保留1位小数);若测定结果x偏大,可能的原因是____________(填序号)。
a.加热温度过高 b.胆矾晶体的颗粒较大 c.加热后放在空气中冷却

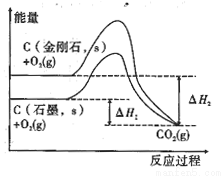
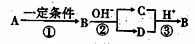
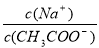 =1
=1
 2CO2(g)+S(l)
2CO2(g)+S(l)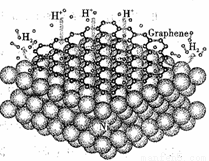
 C,C
C,C C的键能之比最有可能为___________(填序号)。
C的键能之比最有可能为___________(填序号)。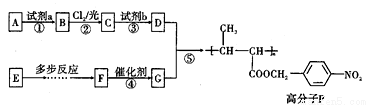
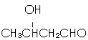 ,以E为起始原料.选用必要的无机试剂合成F,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,以E为起始原料.选用必要的无机试剂合成F,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。