6. 氮氧化物能造成光化学烟雾,引起大气污染,用以下方法可以消除.
氮氧化物能造成光化学烟雾,引起大气污染,用以下方法可以消除.
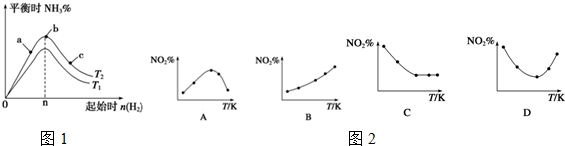
Ⅰ.活性炭还原法处理氮氧化物.若向2L密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应生成甲和乙,甲和乙均为参与大气循环的物质,反应进行到不同时间测得各物质的物质的量浓度如下:
(1)该反应的化学方程式为C+2NO?N2+CO2
(2)T1℃时,该反应的平衡常数K=0.56(保留两位小数)
(3)30min时改变的条件是分离出乙.若30min后升高温度至T2,达到平衡时,容器中NO、甲、乙的浓度之比为2:1:1,则反应的△H<0(填“<”、“=”、“>”).
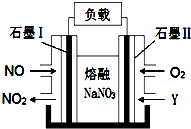
Ⅱ.以NO、O2、熔融NaNO3组成的燃料电池装置如图所示,在使用过程中石墨电极Ⅰ生成NO2.
(4)石墨电极Ⅰ的反应式为NO2+NO3--e-=N2O5;为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,即必须在石墨电极Ⅱ电极处通入一种氧化物Y,Y是N2O5(填物质的化学式).
Ⅲ.CH4催化还原法.已知:
①CH4(g)+4NO2(g)?4NO(g)+CO2(g)+2H2O(l)△H=-622kJ/mol
②CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(l)△H=-955kJ/mol
③H2O(g)=H2O(l)△H=-44.0kJ/mol
(5)写出CH4(g)与NO(g)反应生成N2(g)、CO2(g)和H2O(g)的热化学方程式CH4(g)+4NO(g)?2N2(g)+CO2(g)+2H2O(g)△H=-1200kJ/mol.
(6)恒容时,甲烷与二氧化氮在一定条件下只发生①反应,下列各项中能够判断该反应一定达平衡的是BC(填写正确选项的字母).
A.混合气体的总压强不改变
B.混合气体的相对分子质量不再改变
C.混合气体的密度不再改变
D.v(CH4)正=4v(NO)逆E.c(NO):c(CO2)=4:1.
 氮氧化物能造成光化学烟雾,引起大气污染,用以下方法可以消除.
氮氧化物能造成光化学烟雾,引起大气污染,用以下方法可以消除.Ⅰ.活性炭还原法处理氮氧化物.若向2L密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应生成甲和乙,甲和乙均为参与大气循环的物质,反应进行到不同时间测得各物质的物质的量浓度如下:
浓度(mol/L) 时间(min) | NO | 甲 | 乙 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
(2)T1℃时,该反应的平衡常数K=0.56(保留两位小数)
(3)30min时改变的条件是分离出乙.若30min后升高温度至T2,达到平衡时,容器中NO、甲、乙的浓度之比为2:1:1,则反应的△H<0(填“<”、“=”、“>”).
Ⅱ.以NO、O2、熔融NaNO3组成的燃料电池装置如图所示,在使用过程中石墨电极Ⅰ生成NO2.
(4)石墨电极Ⅰ的反应式为NO2+NO3--e-=N2O5;为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,即必须在石墨电极Ⅱ电极处通入一种氧化物Y,Y是N2O5(填物质的化学式).
Ⅲ.CH4催化还原法.已知:
①CH4(g)+4NO2(g)?4NO(g)+CO2(g)+2H2O(l)△H=-622kJ/mol
②CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(l)△H=-955kJ/mol
③H2O(g)=H2O(l)△H=-44.0kJ/mol
(5)写出CH4(g)与NO(g)反应生成N2(g)、CO2(g)和H2O(g)的热化学方程式CH4(g)+4NO(g)?2N2(g)+CO2(g)+2H2O(g)△H=-1200kJ/mol.
(6)恒容时,甲烷与二氧化氮在一定条件下只发生①反应,下列各项中能够判断该反应一定达平衡的是BC(填写正确选项的字母).
A.混合气体的总压强不改变
B.混合气体的相对分子质量不再改变
C.混合气体的密度不再改变
D.v(CH4)正=4v(NO)逆E.c(NO):c(CO2)=4:1.
5.在100℃时,将N2O4、NO2分别充入两个各为1L的密闭容器中,反应过程中浓度变化如下:(2NO2(g)?N2O4(g)△H<0)
下列说法正确的是( )
| 容器 | 物质 | 起始浓度/(mol•L-1) | 平衡浓度/(mol•L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 | |
| Ⅱ | N2O4 | 0 | 0.014 |
| NO2 | 0.100 | 0.072 |
| A. | 平衡时,Ⅰ、Ⅱ中反应物的转化率α(N2O4)<α(NO2) | |
| B. | 平衡时,Ⅰ、Ⅱ中上述正反应的平衡常数K(Ⅰ)=2K(Ⅱ) | |
| C. | 平衡后,向两容器中分别再充入一定量的NO2,(Ⅰ)中$\frac{c({N}_{2}{O}_{4})}{c(N{O}_{2})}$的值减小,(Ⅱ)$\frac{c({N}_{2}{O}_{4})}{c(N{O}_{2})}$ 的值增大 | |
| D. | 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深 |
4.N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g)?4NO2(g)+O2(g)△H>0T1温度时,向密闭容器中通入N2O5,部分实验数据见下表
下列说法中不正确的是( )
| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
| A. | T1温度下,前500s 以O2表示的反应速率为0.00148mol•L-1•s-1 | |
| B. | 平衡后其他条件不变,将容器的体积压缩到原来的$\frac{1}{2}$,则再平衡时c(N2O5)>5.00 mol•L-1 | |
| C. | T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2 | |
| D. | T1温度下,该反应达到平衡时N2O5的转化率为50% |
2.已知:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98kJ/mol.某温度下,向一体积为2L的密闭容器中充入0.2mol SO2和0.1mol O2,5min达到平衡,放出热量11.76kJ,下列说法正确的是( )
| A. | 5 min内用O2表示的反应速率为0.12 mol/(L•min) | |
| B. | 该反应的平衡常数数值为7.5 | |
| C. | SO2的平衡转化率为60% | |
| D. | 加入催化剂,可使△H变小 |
1.现有容积均为500mL的甲、乙两个密闭容器(甲容器恒温恒容,乙容器恒容绝热),500℃时向两容器中分别充入1mol N2和2.5mol H2,发生反应:N2+3H2═2NH3△H<0并达到平衡.下列有关说法不正确的是( )
| A. | 达平衡后,甲、乙两容器中气体的密度相同 | |
| B. | 甲容器中反应达平衡所需时间比乙容器中的长 | |
| C. | 达平衡后,甲容器中混合气体的平均摩尔质量比乙容器中的大 | |
| D. | 平衡时甲容器中c(N2)=1 mol/L,若再充入1.5 mol N2和1 mol NH3,H2的转化率变大 |
5.下列离子方程式书写正确的是( )
| A. | 向氯化铝溶液中通入过量氨气:4NH3+Al3++2H2O═AlO2-+4NH4+ | |
| B. | 将铝片打磨后置于NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| C. | 向明矾溶液中加入过量的Ba(OH)2溶液:Al3++2SO42-+Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| D. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
4.已知离子的氧化性:Fe3->SO${\;}_{4}^{2-}$,离子的还原性:S2->I->Fe2+,向FeCl3溶液中加入下列物质,溶液颜色不是因发生化学变化而改变的是( )
| A. | SO2 | B. | Na2S | C. | KI | D. | CuSO4 |
3.已知某酸的酸式盐NaHA的水溶液的pH=8,则下列说法中正确的是( )
0 173615 173623 173629 173633 173639 173641 173645 173651 173653 173659 173665 173669 173671 173675 173681 173683 173689 173693 173695 173699 173701 173705 173707 173709 173710 173711 173713 173714 173715 173717 173719 173723 173725 173729 173731 173735 173741 173743 173749 173753 173755 173759 173765 173771 173773 173779 173783 173785 173791 173795 173801 173809 203614
| A. | 在Na2A、NaHA、H2A的溶液中所存在的阴离子种类不同 | |
| B. | 在NaHA溶液离子浓度大小顺序为:c(Na+)>c(A-)>c(HA-)>c(OH-)>c(H+) | |
| C. | 相同物质的量浓度的Na2A和NaHA溶液,前者pH大于后者 | |
| D. | HA-的水解方程式为:HA-+H2O?A-+H3O- |