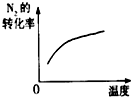
5.在一个容积固定为2L的密闭容器中,发生反应aA(g)+bB(g)?pC(g)△H=?反应情况记录如表:
请仔细分析表中数据,回答下列问题:
(1)p=2,a=1,b=2(取最小整数)
(2)第2min到第4min内,A的平均反应速率v(A)=0.2 mol•L-1•min-1
(3)若从开始到第4min建立平衡时,反应放出的热量为234kJ,则该反应的△H=-195.
| 时间 | c(A)/(mol•L-1) | c(B)/(mol•L-1) | c(C)/(mol•L-1) |
| 0min | 1 | 3 | 0 |
| 第2min | 0.8 | 2.6 | 0.4 |
| 第4min | 0.4 | 1.8 | 1.2 |
| 第6min | 0.4 | 1.8 | 1.2 |
(1)p=2,a=1,b=2(取最小整数)
(2)第2min到第4min内,A的平均反应速率v(A)=0.2 mol•L-1•min-1
(3)若从开始到第4min建立平衡时,反应放出的热量为234kJ,则该反应的△H=-195.
4.下列各组比较中,前者比后者大的是( )
| A. | 25℃时,pH均为2的H2SO4溶液和盐酸中氢离子的物质的量浓度 | |
| B. | 同温度、同浓度的NaCl溶液和氨水的导电能力 | |
| C. | 25℃时,pH均为2的盐酸和CH3COOH溶液中溶质的物质的量浓度 | |
| D. | 25℃时,pH为3的盐酸和pH为11的Ba(OH)2溶液中水的电离程度 |
3.下列如图所示装置,肯定不符合气密性要求的是( )
| A. | 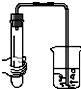 | B. | 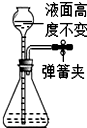 | C. | 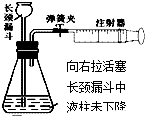 | D. | 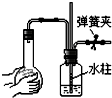 |
1.下列关于水的说法正确的是( )
| A. | 我们平时应多饮用不二门的水 | |
| B. | 所有天然水都不能饮用 | |
| C. | 人体内含有约$\frac{2}{3}$体重的水,故人每天不用喝水也可 | |
| D. | 人体需要不断补充水分,每人每天需要补充水 |
20.在一个体积固定的密闭容器中加入2mol A和1mol B,发生反应:2A(g)+B(g)?3C(g)+D(g),达到平衡时C的浓度为a mol/L.若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为a mol/L的是( )
| A. | 4 mol A+2 mol B | B. | 2 mol A+1 mol B+1 mol He | ||
| C. | 3 mol C+2 mol D | D. | 2 mol A+1 mol D |
19.下列热化学方程式书写正确的是(△H的绝对值均正确)( )
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol(燃烧热) | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热) | |
| C. | 2NO2=O2+2NO△H=+116.2kJ/mol(反应热) | |
| D. | S(s)+O2(g)═SO2(g)△H=-296.8kJ/mol(反应热) |
18.溶液、胶体和浊液这三种分散系的根本区别是( )
| A. | 能否透过滤纸 | B. | 能否发生丁达尔效应 | ||
| C. | 分散质粒子的大小 | D. | 是否均一、透明、稳定 |
17.为了达到下表中所列的一些有关家庭常用物质的实验要求,请选择合适的化学试剂,将其标号填入对应的空格中.
供选择的化学试剂:
A.新制氢氧化铜悬浊液 B.硝酸银溶液和硝酸
C.碘水 D.无水硫酸铜粉末.
0 173584 173592 173598 173602 173608 173610 173614 173620 173622 173628 173634 173638 173640 173644 173650 173652 173658 173662 173664 173668 173670 173674 173676 173678 173679 173680 173682 173683 173684 173686 173688 173692 173694 173698 173700 173704 173710 173712 173718 173722 173724 173728 173734 173740 173742 173748 173752 173754 173760 173764 173770 173778 203614
| 实验要求 | 化学试剂 |
| 检验酒精中是否有水 | D |
| 区别蔗糖和葡萄糖 | A |
| 证明地瓜中有淀粉 | C |
| 证明味精中有NaCl | B |
A.新制氢氧化铜悬浊液 B.硝酸银溶液和硝酸
C.碘水 D.无水硫酸铜粉末.