题目内容
2.下列物质能导电是①⑤,属于电解质是②③④,属于非电解质的是⑥.(填序号,多选或错选扣分)①水银 ②烧碱 ③硫酸钡 ④氯化钠晶体 ⑤盐酸 ⑥蔗糖.
分析 金属、部分非金属、电解质溶液和熔融的电解质可以导电;
溶于水或熔融状态下能够电离出阴阳离子的化合物是电解质;
溶于水和熔融状态下都不能够电离出阴阳离子的化合物是非电解质;
解答 解:能导电的物质有金属、电解质溶液或熔融液,即含有自由移动离子或电子的物质能够导电,符合条件的有:①⑤,
电解质是在水溶液或熔融状态下能导电的化合物,符合条件的有:②③④,
非电解质是在水溶液和熔融状态下均不能导电的化合物,符合条件的有:⑥,
故答案为:①⑤;②③④;⑥.
点评 本题主要考查了电解质与非电解质的概念、粒子的导电性,题目难度不大,注意电解质和导电性的关系,导电的不一定是电解质,电解质不是任何条件下都导电.

练习册系列答案
相关题目
13.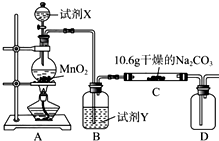 某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质.
某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质.
(1)装置A中发生反应的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)装置B中试剂Y应为饱和食盐水.
(3)该实验装置中明显存在不足之处,改进的措施为在装置D后连接一尾气处理装置.
(4)已知在装置C中通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体(含氯氧化物).C中含氯元素的盐只有一种,且含有NaHCO3.现对C中的成分进行猜想和探究.
①提出合理假设.
假设一:存在两种成分,为NaHCO3和NaCl;
假设二:存在三种成分,为NaHCO3和NaCl、Na2CO3.
②设计方案并实验.请在表格中写出实验步骤以及预期现象和结论.
限选试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯.
结论:由步骤3的结论结合步骤2中的a,则假设一成立;由步骤3的结论结合步骤2中的b,则假设二成立.
(5)已知C中有0.1mol Cl2参加反应.若假设一成立,可推知C中反应生成的含氯氧化物为Cl2O(写化学式).
 某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质.
某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质.(1)装置A中发生反应的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)装置B中试剂Y应为饱和食盐水.
(3)该实验装置中明显存在不足之处,改进的措施为在装置D后连接一尾气处理装置.
(4)已知在装置C中通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体(含氯氧化物).C中含氯元素的盐只有一种,且含有NaHCO3.现对C中的成分进行猜想和探究.
①提出合理假设.
假设一:存在两种成分,为NaHCO3和NaCl;
假设二:存在三种成分,为NaHCO3和NaCl、Na2CO3.
②设计方案并实验.请在表格中写出实验步骤以及预期现象和结论.
限选试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯.
结论:由步骤3的结论结合步骤2中的a,则假设一成立;由步骤3的结论结合步骤2中的b,则假设二成立.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取C中的少量固体样品于试管中,滴加足量蒸馏水 至固体溶解,然后将所得溶液分别置于A、B试管中. | |
| 步骤2:向A试管中滴加适量BaCl2溶液. | a.a.若无明显现象,证明固体中不含Na2CO3 b.若溶液变浑浊,证明固体中含Na2CO3 |
| 步骤3:向B试管中滴加过量的稀硝酸,再滴加AgNO3溶液(填写所加试剂即可) | b.若溶液变浑浊,证明固体中含有NaCl |
10.某无土栽培用的营养液要求KCl、K2SO4、NH4Cl三种固体原料的物质的量之比为1:4:8,若用696g K2SO4配成1L营养液,关于该营养液的说法正确的是( )
| A. | 所需KCl和NH4Cl的质量分别为:74.5g和428g | |
| B. | 所配营养液K+的物质的量浓度为8 mol/L | |
| C. | 若用1000mL的容量瓶配制,定容时俯视刻度线,所配营养液浓度偏低 | |
| D. | 所用的容量瓶除检查是否漏水外,容量瓶要保持干燥 |
17.为了达到下表中所列的一些有关家庭常用物质的实验要求,请选择合适的化学试剂,将其标号填入对应的空格中.
供选择的化学试剂:
A.新制氢氧化铜悬浊液 B.硝酸银溶液和硝酸
C.碘水 D.无水硫酸铜粉末.
| 实验要求 | 化学试剂 |
| 检验酒精中是否有水 | D |
| 区别蔗糖和葡萄糖 | A |
| 证明地瓜中有淀粉 | C |
| 证明味精中有NaCl | B |
A.新制氢氧化铜悬浊液 B.硝酸银溶液和硝酸
C.碘水 D.无水硫酸铜粉末.
7.为了使FeCl3溶液中$\frac{c(F{e}^{3+})}{c(c{l}^{-})}$增大,可加入的物质是( )
| A. | 适量的HCl气体 | B. | 适量的硫酸氢钠 | C. | 适量的NaOH固体 | D. | 适量的稀HNO3 |
11.下列说法中,不正确的是( )
| A. | 电解质的电离,既是化学过程,也是化学反应 | |
| B. | 即使没有发生化学变化,也可能有能量的变化 | |
| C. | 化学反应中既有物质变化又有能量变化 | |
| D. | 物质的化学能可以通过不同的变化方式转化为热能、电能等 |
12.氯水中有Cl2、HCl、HClO,其中含量最多的是( )
| A. | HCl | B. | HClO | C. | Cl2 | D. | 不能确定 |