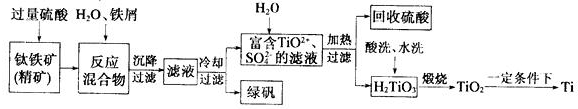
8.为测定一置于空气中的某硫酸酸化的FeSO4溶液中Fe2+被氧化的百分率,某同学准确量取pH=1(忽略Fe2+、Fe3+的水解)的FeSO4溶液200mL,加入过量BaCl2溶液,充分反应后过滤、洗涤、干燥,得到沉淀28.0g;再另取同样的FeSO4溶液200mL,向其中加入过量NaOH溶液,搅拌使其充分反应,待沉淀全部变为红褐色后,过滤、洗涤并灼烧所得固体,最终得固体8.0g.
(1)写出反应中涉及的化学方程式(至少3个)
(2)通过计算,填写下表:
注:c(Fe2+、Fe3+)表示Fe2+和Fe3+的总的物质的量的浓度
(3)计算原溶液中Fe2+被氧化的百分率.
(1)写出反应中涉及的化学方程式(至少3个)
(2)通过计算,填写下表:
| c(H+) | c(SO42-) | c(Fe2+、Fe3+) |
(3)计算原溶液中Fe2+被氧化的百分率.
4.三氯化磷(PCl3)是一种重要的掺杂剂.实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如图所示:(部分夹持装置略去)

已知:①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;
②PCl3遇水会强烈水解生成 H3PO3和气体;
③PCl3遇O2会生成POCl3,POCl3溶于PCl3;
④PCl3、POCl3的熔沸点见下表:
请回答下列问题:
(1)B中所装试剂是浓硫酸;
E中冷水的作用是冷凝PCl3防止其挥发.
(2)F中碱石灰的作用是吸收多余的氯气,防止空气中的水蒸汽进入烧瓶中和PCl3 反应.
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是排尽装置中的空气,防止白磷自燃.
(4)粗产品中常含有POC13、PCl5等.加入黄磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.
(5)实验结束时,可以利用C中的试剂吸收多余的氯气,C中反应的离子方程式为Cl2+2OH-=Cl-+ClO-+2H2O.
(6)通过下面方法可测定产品中PCl3的质量分数:
①迅速称取1.00g产品,加水反应后配成250mL溶液;
②取以上溶液25.00mL,向其中加入10.00mL 0.1000mol/L碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol/L的Na2S2O3,溶液滴定;
④重复②、③操作,平均消耗Na2S2O3溶液8.40mL.
已知:H3PO3+I2=H3PO4+2HI,I2+2Na2S2O3═2NaI+Na2S4O6,根据上述数据,假设测定过程中没有其他反应,该产品中PCl3的质量分数为79.75%.

已知:①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;
②PCl3遇水会强烈水解生成 H3PO3和气体;
③PCl3遇O2会生成POCl3,POCl3溶于PCl3;
④PCl3、POCl3的熔沸点见下表:
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
(1)B中所装试剂是浓硫酸;
E中冷水的作用是冷凝PCl3防止其挥发.
(2)F中碱石灰的作用是吸收多余的氯气,防止空气中的水蒸汽进入烧瓶中和PCl3 反应.
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是排尽装置中的空气,防止白磷自燃.
(4)粗产品中常含有POC13、PCl5等.加入黄磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.
(5)实验结束时,可以利用C中的试剂吸收多余的氯气,C中反应的离子方程式为Cl2+2OH-=Cl-+ClO-+2H2O.
(6)通过下面方法可测定产品中PCl3的质量分数:
①迅速称取1.00g产品,加水反应后配成250mL溶液;
②取以上溶液25.00mL,向其中加入10.00mL 0.1000mol/L碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol/L的Na2S2O3,溶液滴定;
④重复②、③操作,平均消耗Na2S2O3溶液8.40mL.
已知:H3PO3+I2=H3PO4+2HI,I2+2Na2S2O3═2NaI+Na2S4O6,根据上述数据,假设测定过程中没有其他反应,该产品中PCl3的质量分数为79.75%.
3.钴是重要的战略金属元素,钴及其化合物在化工、机械、航空和军事等部门具有广泛的应用.以水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等杂质)制取CoC2O4的工艺流程如图1:
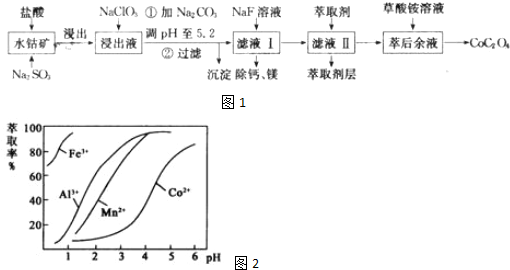
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
(1)浸出过程中加入Na2SO3的目的是将Fe3+、Co3+(填离子符号)还原,若只用盐酸浸取,则会产生污染空气的有毒气体,反应的离子方程式为2Co3++2Cl-=Cl2 ↑+2Co2+.
(2)向浸出液中加入NaClO3的作用是将Fe2+氧化成Fe3+,反应的离子方程式为ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O.
(3)浸出液中加Na2CO3调pH至5.2时生成的沉淀为Fe(OH)3、Al(OH)3(填化学式),能够生成此沉淀的原因是铝离子、铁离子能与碳酸根离子发生双水解生成沉淀和二氧化碳,反应的离子方程式为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2、2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑(用离子方程式结合必要的文字说明).
(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知KSp( MgF2)=7.35
×10-ll、Ksp( CaF2)=1.05×10-10,当加入过量NaF后,所得滤液中$\frac{c(M{g}^{2+})}{c(C{a}^{2+})}$=0.7
(5)滤液Ⅱ中加入萃取剂的作用是除去溶液中的Mn2+,萃取剂对金属离子的萃取率与pH的关系如图2所
示.使用萃取剂适宜的pH是B(填字母).
a.接近2.0
b.接近3.0
c.接近4.0.

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入Na2SO3的目的是将Fe3+、Co3+(填离子符号)还原,若只用盐酸浸取,则会产生污染空气的有毒气体,反应的离子方程式为2Co3++2Cl-=Cl2 ↑+2Co2+.
(2)向浸出液中加入NaClO3的作用是将Fe2+氧化成Fe3+,反应的离子方程式为ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O.
(3)浸出液中加Na2CO3调pH至5.2时生成的沉淀为Fe(OH)3、Al(OH)3(填化学式),能够生成此沉淀的原因是铝离子、铁离子能与碳酸根离子发生双水解生成沉淀和二氧化碳,反应的离子方程式为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2、2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑(用离子方程式结合必要的文字说明).
(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知KSp( MgF2)=7.35
×10-ll、Ksp( CaF2)=1.05×10-10,当加入过量NaF后,所得滤液中$\frac{c(M{g}^{2+})}{c(C{a}^{2+})}$=0.7
(5)滤液Ⅱ中加入萃取剂的作用是除去溶液中的Mn2+,萃取剂对金属离子的萃取率与pH的关系如图2所
示.使用萃取剂适宜的pH是B(填字母).
a.接近2.0
b.接近3.0
c.接近4.0.
20.一氧化碳、甲醛、二氧化硫均有毒,均是常见的大气污染物.
(1)人们常用催化剂来选择反应进行的方向,如图1为一定条件下1 molCH3OH与O2发生反应时,生成CO或CO2或HCHO的能量变化[反应物O2(g)和生成物H2O(g)已略去].
①在有催化剂的作用下,CH3OH与O2反应的主要产物是HCHO(填“CO”“CO2”或“HCHO”).
②2HCHO(g)+O2(g)=2CO(g)+2H2O(g)△H=-470KJ•mol-1.
(2)煤炭中的硫主要以黄铁矿的形式存在,用氢气脱出黄铁矿中硫的相关反应见下表,其相关反应的平衡常数的对数值与温度的关系如图2.
①上述反应中,△H1>(填“>”或“<”)0.
②提高硫的脱除率可采取的措施有升高温度(任填一种).
③1000K时,向2L恒容密闭容器中充入一定量的H2(g)和FeS2(g),只发生反应①,达到平衡时,H2的转化率为99%.
(3)用细菌冶炼铜时,当黄铜矿中伴有黄铁矿时,可明显提高浸取速率,其原理如图3.
①冶炼过程中,正极周围溶液的pH增大(填“增大”“减小”或“不变”).
②负极产生单质硫的电极反应式为CuFeS2-4e-=Cu2++Fe2++2S.
0 173479 173487 173493 173497 173503 173505 173509 173515 173517 173523 173529 173533 173535 173539 173545 173547 173553 173557 173559 173563 173565 173569 173571 173573 173574 173575 173577 173578 173579 173581 173583 173587 173589 173593 173595 173599 173605 173607 173613 173617 173619 173623 173629 173635 173637 173643 173647 173649 173655 173659 173665 173673 203614
(1)人们常用催化剂来选择反应进行的方向,如图1为一定条件下1 molCH3OH与O2发生反应时,生成CO或CO2或HCHO的能量变化[反应物O2(g)和生成物H2O(g)已略去].
①在有催化剂的作用下,CH3OH与O2反应的主要产物是HCHO(填“CO”“CO2”或“HCHO”).
②2HCHO(g)+O2(g)=2CO(g)+2H2O(g)△H=-470KJ•mol-1.

(2)煤炭中的硫主要以黄铁矿的形式存在,用氢气脱出黄铁矿中硫的相关反应见下表,其相关反应的平衡常数的对数值与温度的关系如图2.
| 相关反应 | 反应热 | 平衡常数K |
| ①FeS2(s)+H2(g)?FeS(s)+H2S(g) | △H1 | K1 |
| ②$\frac{1}{2}$FeS2(s)+H2(g)?$\frac{1}{2}$FeS(s)+H2S(g) | △H2 | K2 |
| ③FeS(s)+H2(g)?Fe(s)+H2S(g) | △H3 | K3 |
②提高硫的脱除率可采取的措施有升高温度(任填一种).
③1000K时,向2L恒容密闭容器中充入一定量的H2(g)和FeS2(g),只发生反应①,达到平衡时,H2的转化率为99%.
(3)用细菌冶炼铜时,当黄铜矿中伴有黄铁矿时,可明显提高浸取速率,其原理如图3.
①冶炼过程中,正极周围溶液的pH增大(填“增大”“减小”或“不变”).
②负极产生单质硫的电极反应式为CuFeS2-4e-=Cu2++Fe2++2S.

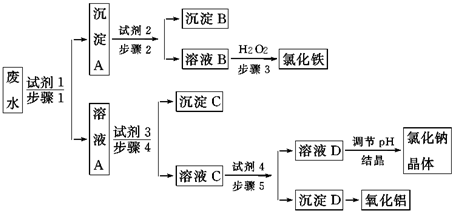
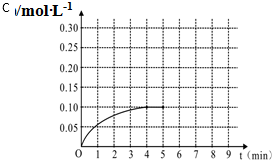 一定温度下,将0.4mol SO2和0.2mol O2放入固定容积为2L的密闭容器中,发生反应2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ/mol,反应中SO3的物质的量浓度的变化情况如图:
一定温度下,将0.4mol SO2和0.2mol O2放入固定容积为2L的密闭容器中,发生反应2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ/mol,反应中SO3的物质的量浓度的变化情况如图: