19.下列离子方程式正确的是( )
| A. | 用石墨作电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+Cl2↑+H2↑ | |
| B. | Fe3O4与过量的稀HNO3反应:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| C. | 向Ba(OH)2 溶液中逐滴加入NaHSO4溶液至溶液恰好为中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | Na2S溶液呈碱性:S2-+2H2O?H2S+2OH- |
16.下列关于AgCl沉淀溶解平衡的说法正确的是( )
| A. | 升高温度,AgCl沉淀的溶解度减小 | |
| B. | AgCl难溶于水,溶液中没有Ag+和Cl- | |
| C. | Ag+与Cl-结合成AgCl的速率与AgCl溶解的速率相等 | |
| D. | 向AgCl饱和溶液中加入NaCl固体,AgCl沉淀的溶解度不变 |
15.碳、氮广泛的分布在自然界中,碳、氮的化合物性能优良,在工业生产和科技领域有重要用途.
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700°C的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)△H=-1591.2kJ/mol,则该反应每转移1mole-,可放出的热量为132.6kJ.
(2)高温时,用CO还原MgSO4可制备高纯MgO.
①750℃时,测得气体中含等物质的量的SO2和SO3,此时反应的化学方程式是CO+2MgSO4 $\frac{\underline{\;高温\;}}{\;}$2MgO+CO2+SO2+SO3.
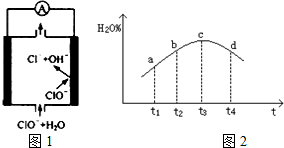
②由MgO制成的Mg可构成“镁-次氯酸盐”电池,其装置示意图如图1,该电池的正极反应式为ClO-+2e-+H2O=Cl-+2OH-.
(3)某研究小组将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下数据:
①实验Ⅰ中,前5min的反应速率v(CO2)=0.15mol/(L.min).
②下列能判断实验Ⅱ已经达到平衡状态的是(填写选项序号)ad.
a.容器内CO、H2O、CO2、H2的浓度不再变化 b.容器内压强不再变化
c.混合气体的密度保持不变 d.v正(CO)=v逆(CO2)
e.容器中气体的平均相对分子质量不随时间而变化
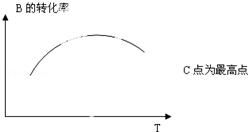
③若实验Ⅲ的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如图2所示,b点v正>v逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是该反应达到平衡后,因反应为放热反应且反应容器为绝热容器,故容器内温度升高,反应逆向进行.

(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700°C的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)△H=-1591.2kJ/mol,则该反应每转移1mole-,可放出的热量为132.6kJ.
(2)高温时,用CO还原MgSO4可制备高纯MgO.
①750℃时,测得气体中含等物质的量的SO2和SO3,此时反应的化学方程式是CO+2MgSO4 $\frac{\underline{\;高温\;}}{\;}$2MgO+CO2+SO2+SO3.
②由MgO制成的Mg可构成“镁-次氯酸盐”电池,其装置示意图如图1,该电池的正极反应式为ClO-+2e-+H2O=Cl-+2OH-.
(3)某研究小组将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
| CO | H2O | CO | H2 | |||
| 1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
| 2 | 900 | 1 | 2 | 0.5 | 0.5 | - |
②下列能判断实验Ⅱ已经达到平衡状态的是(填写选项序号)ad.
a.容器内CO、H2O、CO2、H2的浓度不再变化 b.容器内压强不再变化
c.混合气体的密度保持不变 d.v正(CO)=v逆(CO2)
e.容器中气体的平均相对分子质量不随时间而变化
③若实验Ⅲ的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如图2所示,b点v正>v逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是该反应达到平衡后,因反应为放热反应且反应容器为绝热容器,故容器内温度升高,反应逆向进行.
14. 某研究小组向2L密闭容器中加入一定量的固体A和气体B发生反应:
某研究小组向2L密闭容器中加入一定量的固体A和气体B发生反应:
A(s)+2B(g)?D(g)+E(g)△H=Q kJ•mol-1.在T1℃时,反应进行到不同时间测得各物质的物质的量如表:
(1)T1℃时,该反应的平衡常数K=0.25;
(2)30min后,只改变某一条件,反应重新达到平衡,根据表中的数据判断改变的条件可能是ad(填字母编号).
a.通入一定量的B b.加入一定量的固体A
c.升高反应体系温度 d.同时加入0.2molB、0.1molD、0.1molE
(3)维持容器的体积和温度T1不变,当向该容器中加入1.60molB、0.20molD、0.20molE和n molA,达到平衡后,与表格中20分钟时各物质的浓度完全相同时,则投入固体A的物质的量n应不少于0.3mol.
(4)维持容器的体积和温度T1不变,各物质的起始物质的量为:n(A)=1.0mol,n(B)=3.0mol,n(D)=amol,n(E)=0mol,达到平衡后,n(E)=0.50mol,则a=1.5.
(5)若该密闭容器绝热,实验测得B的转化率B%随温度变化的示意图如图所示.由图可知,Q<0 (填<、>、=),c点v(正)=v(逆)(填<、>、=).
0 173380 173388 173394 173398 173404 173406 173410 173416 173418 173424 173430 173434 173436 173440 173446 173448 173454 173458 173460 173464 173466 173470 173472 173474 173475 173476 173478 173479 173480 173482 173484 173488 173490 173494 173496 173500 173506 173508 173514 173518 173520 173524 173530 173536 173538 173544 173548 173550 173556 173560 173566 173574 203614
 某研究小组向2L密闭容器中加入一定量的固体A和气体B发生反应:
某研究小组向2L密闭容器中加入一定量的固体A和气体B发生反应:A(s)+2B(g)?D(g)+E(g)△H=Q kJ•mol-1.在T1℃时,反应进行到不同时间测得各物质的物质的量如表:
时间(min) | 0 | 10 | 20 | 30 | 40 | 50 |
| B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
| D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
| E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
(2)30min后,只改变某一条件,反应重新达到平衡,根据表中的数据判断改变的条件可能是ad(填字母编号).
a.通入一定量的B b.加入一定量的固体A
c.升高反应体系温度 d.同时加入0.2molB、0.1molD、0.1molE
(3)维持容器的体积和温度T1不变,当向该容器中加入1.60molB、0.20molD、0.20molE和n molA,达到平衡后,与表格中20分钟时各物质的浓度完全相同时,则投入固体A的物质的量n应不少于0.3mol.
(4)维持容器的体积和温度T1不变,各物质的起始物质的量为:n(A)=1.0mol,n(B)=3.0mol,n(D)=amol,n(E)=0mol,达到平衡后,n(E)=0.50mol,则a=1.5.
(5)若该密闭容器绝热,实验测得B的转化率B%随温度变化的示意图如图所示.由图可知,Q<0 (填<、>、=),c点v(正)=v(逆)(填<、>、=).
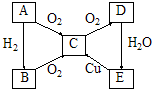 A,B,C,D,E五种物质可按图所示发生转变(反应条件已略去).
A,B,C,D,E五种物质可按图所示发生转变(反应条件已略去).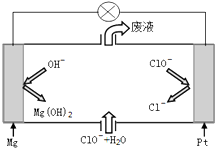 硫酸盐主要来自地层矿物质,多以硫酸钙、硫酸镁的形态存在,硫酸盐有着许多重要的应用.
硫酸盐主要来自地层矿物质,多以硫酸钙、硫酸镁的形态存在,硫酸盐有着许多重要的应用.