12.向H2SO4、CuCl2混合溶液中投入足量的铁粉,经充分反应后,过滤、洗涤、干燥、称重,知所得固体的质量与加入的铁粉的质量相等,则原溶液中c(SO42-)与c(Cl-)之比( )
| A. | 1:2 | B. | 1:7 | C. | 7:1 | D. | 1:14 |
11.在下列变化中,需要加入合适的氧化剂才能实现的是( )
| A. | Fe→Fe3+ | B. | CO2→CO | C. | Na2O2→O2 | D. | CuO→Cu2+ |
10.下列图示中正确的实验操作是( )
| A. |  除去CO中的CO2 | B. |  萃取时振荡混合液 | ||
| C. | 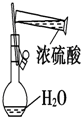 配制浓硫酸 | D. | 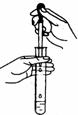 向试管中滴加液体 |
9.在三个密闭容器中分别充入氦气、氧气、氮气,当它们的温度和密度都相同时,这三种气体的压强(P)从大到小的顺序是( )
| A. | 氦气>氧气>氮气 | B. | 氧气>氮气>氦气 | C. | 氧气>氦气>氮气 | D. | 氦气>氮气>氧气 |
8.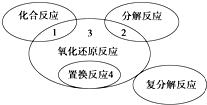 氧化还原反应与四种基本反应类型的关系如图,则下列化学反应属于区域3的是( )
氧化还原反应与四种基本反应类型的关系如图,则下列化学反应属于区域3的是( )
 氧化还原反应与四种基本反应类型的关系如图,则下列化学反应属于区域3的是( )
氧化还原反应与四种基本反应类型的关系如图,则下列化学反应属于区域3的是( )| A. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | B. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | ||
| C. | CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$ Cu+CO2 | D. | Zn+H2SO4═ZnSO4+H2↑ |
7.化学是一门以实验为基础的学科,掌握基本实验方法和操作技能是做好化学实验的基础.下列有关说法错误的是( )
| A. | 元素分析仪可以确定物质中是否含有C、H、O、N、Cl、Br等元素 | |
| B. | 用红外光谱仪可以确定物质中是否存在某些有机原子团 | |
| C. | 用原子吸收光谱可以确定物质中含有哪些金属元素 | |
| D. | 焰色反应适用于所有金属元素的鉴别 |
5.用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.2000mol•L -1的氢氧化钠溶液(指示剂为酚酞),滴定结果如下:
(1)根据以上数据可以计算出盐酸的物质的量浓度为0.1448mol•L-1.
(2)达到滴定终点的标志是无色变粉红色且30s不变色.
(3)以下操作造成测定结果偏高的原因可能是ADE.
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管.
| NaOH起始读数 | NaOH终点读数 | |
| 第一次 | 0.10mL | 18.60mL |
| 第二次 | 0.30mL | 18.00mL |
(2)达到滴定终点的标志是无色变粉红色且30s不变色.
(3)以下操作造成测定结果偏高的原因可能是ADE.
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管.
4.现有下列四个图象:

下列反应中全部符合上述图象的反应是( )

下列反应中全部符合上述图象的反应是( )
| A. | N2(g)+3H2(g)?2NH3(g)△H1<0 | B. | 2SO3(g)?2SO2(g)+O2(g)△H2>0 | ||
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H3<0 | D. | H2(g)+CO(g)?C(s)+H2O(g)△H4>0 |
3.25℃时,0.05mol/L的Ba(OH)2溶液,pH为( )
0 172921 172929 172935 172939 172945 172947 172951 172957 172959 172965 172971 172975 172977 172981 172987 172989 172995 172999 173001 173005 173007 173011 173013 173015 173016 173017 173019 173020 173021 173023 173025 173029 173031 173035 173037 173041 173047 173049 173055 173059 173061 173065 173071 173077 173079 173085 173089 173091 173097 173101 173107 173115 203614
| A. | 12.7 | B. | 12.0 | C. | 13.0 | D. | 13.7 |