11.已知在K2Cr2O7的溶液中存在如下平衡:
Cr2O72-+H2O?2CrO42-+2H+ K2Cr2O7为橙色,K2 CrO4为黄色.取两只试管各加入5ml0.1mol/L K2Cr2O7溶液,然后按如表步骤操作.
回答:(1)本实验除试管外还必须使用的一种玻璃仪器是:胶头滴管.
(2)1号实验的现象是:溶液橙色加深;结论是:增大生成物浓度平衡向逆方向移动;
(3)2号实验的现象是:溶液黄色加深;结论是:减小生成物浓度平衡向正方向移动.
Cr2O72-+H2O?2CrO42-+2H+ K2Cr2O7为橙色,K2 CrO4为黄色.取两只试管各加入5ml0.1mol/L K2Cr2O7溶液,然后按如表步骤操作.
| 编号 | 1 | 2 |
| 步骤 | 滴加3~10滴浓硫酸 | 滴加10~20滴6mol/LNaOH溶液 |
(2)1号实验的现象是:溶液橙色加深;结论是:增大生成物浓度平衡向逆方向移动;
(3)2号实验的现象是:溶液黄色加深;结论是:减小生成物浓度平衡向正方向移动.
10.对标准状况下的四种气体的关系从小到大表示不正确的是( )
①6.72L甲烷 ②3.01×1023HCl分子 ③13.6g H2S ④0.2mol NH3.
①6.72L甲烷 ②3.01×1023HCl分子 ③13.6g H2S ④0.2mol NH3.
| A. | 质量:④<①<③<② | B. | 密度:①<④<③<② | ||
| C. | 体积:④<①<②<③ | D. | 氢原子数:②<④<③<① |
9.下列说法正确是( )
| A. | 电解质在水中发生了的电离,产生了能够自由移动的离子 | |
| B. | 酸性氧化物都是非金属元素形成的氧化物 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 只含一种元素的阳离子与另一种元素的阴离子所组成的物质一定是纯净物 |
8.下列有关实验的说法中正确的是( )
| A. | 在利用重结晶的方法制备KNO3的过程中,可在漏斗中加入酒精来洗涤 | |
| B. | 在石油的分馏实验中,冷凝管中冷水应从上口进入,热水从下口流出 | |
| C. | 粗盐提纯中,在溶解粗盐时,应用大量的水来溶解,以防止食盐不完全溶解 | |
| D. | 在分液实验中,待液体静置分层后,上、下层液体都应分别从分液漏斗下端的活塞放出 |
7.下列仪器经常用于物质分离的有( )
①漏斗 ②试管 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥容量瓶 ⑦蒸发皿 ⑧坩埚.
①漏斗 ②试管 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥容量瓶 ⑦蒸发皿 ⑧坩埚.
| A. | ①③⑤⑥ | B. | ①②④⑥ | C. | ①③⑤⑦ | D. | ①③⑥⑧ |
6.古诗词是古人为我们留下的宝贵精神财富.下列诗句不涉及氧化还原反应的是( )
| A. | 野火烧不尽,春风吹又生 | B. | 春蚕到死丝方尽,蜡炬成灰泪始干 | ||
| C. | 爆竹声中一岁除,春风送暖入屠苏 | D. | 粉身碎骨浑不怕,要留清自在人间 |
5.下列物质分类正确的是( )
| A. | HCl、纯碱、硫酸钡均为强电解质 | |
| B. | SO2、SiO2、CO均为酸性氧化物 | |
| C. | 稀豆浆、油水、氯化铁溶液均为胶体 | |
| D. | 大理石、CuSO4•5H2O、氨水均为混合物 |
4.己知金属钾投入水中会发生剧烈反应,并有氢气生成.运输金属钾的包装箱应贴有的图标是( )
| A. |  易燃液体 | B. |  遇湿易燃物品 | C. |  氧化剂 | D. |  腐蚀品 |
3.根据反应(1)→(4),可以判断下列4个物质的氧化性由强到弱的正确顺序是( )
(1)Cl2+2KI=2KCl+I2;
(2)2FeCl2+Cl2=2FeCl3;
(3)2FeCl3+2HI=2FeCl2+2HCl+I2,
(4)H2S+I2=S+2HI.
0 172911 172919 172925 172929 172935 172937 172941 172947 172949 172955 172961 172965 172967 172971 172977 172979 172985 172989 172991 172995 172997 173001 173003 173005 173006 173007 173009 173010 173011 173013 173015 173019 173021 173025 173027 173031 173037 173039 173045 173049 173051 173055 173061 173067 173069 173075 173079 173081 173087 173091 173097 173105 203614
(1)Cl2+2KI=2KCl+I2;
(2)2FeCl2+Cl2=2FeCl3;
(3)2FeCl3+2HI=2FeCl2+2HCl+I2,
(4)H2S+I2=S+2HI.
| A. | S>I2>Fe3+>Cl2 | B. | Cl2>Fe3+>I2>S | C. | Fe3+>Cl2>S>I2 | D. | Cl2>I2>Fe3+>S |
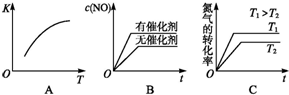 汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)?2NO(g)△H>0已知该反应在2404℃时,平衡常数K=64×10-4.请回答:
汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)?2NO(g)△H>0已知该反应在2404℃时,平衡常数K=64×10-4.请回答: