10.已知反应:2CH3OH(g)?CH3OCH3(g)+H2O(g),某温度下的平衡常数为400.在此温度下,向密闭容器中加入一定量CH3OH,反应到5min时测得各组分的浓度如表所示:
(1)该反应在低温下(此时水为液态)能自发进行,则该反应的△H<0 (填“>”、“<”或“=”,下同).
(2)比较此时正、逆反应速率的大小:v正>v逆,理由是浓度商Qc=$\frac{0.6×0.6}{0.4{4}^{2}}$=1.36<K=400,反应向正反应进行.
(3)前5min时,用CH3OCH3表示该反应的速率为0.12mol/(L.min).
(4)再过一段时间后,反应达到平衡状态.能判断该反应已达到化学平衡状态的依据是B(填字母).
A.容器中压强不变 B.混合气体中c(CH3OH)不变
C.v生成(CH3OH)=2v消耗(H2O) D.c(CH3OCH3)=c (H2O)
(5)达到平衡状态时,CH3OH的转化率97.6%(计算结果保留到小数点后1位).
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
(2)比较此时正、逆反应速率的大小:v正>v逆,理由是浓度商Qc=$\frac{0.6×0.6}{0.4{4}^{2}}$=1.36<K=400,反应向正反应进行.
(3)前5min时,用CH3OCH3表示该反应的速率为0.12mol/(L.min).
(4)再过一段时间后,反应达到平衡状态.能判断该反应已达到化学平衡状态的依据是B(填字母).
A.容器中压强不变 B.混合气体中c(CH3OH)不变
C.v生成(CH3OH)=2v消耗(H2O) D.c(CH3OCH3)=c (H2O)
(5)达到平衡状态时,CH3OH的转化率97.6%(计算结果保留到小数点后1位).
9.水煤气 (主要成分:CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C (s)+H2O(g)?CO (g)+H2 (g);△H=+131.3kJ•mol-1
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中相应的空格.
(2)另有一个容积可变的密闭容器.恒温恒压下,向其中加入1.0mol炭和 1.0mo l水蒸气 (H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍.平衡时水蒸气的转化率为25%;向该容器中补充 a mol 炭,水蒸气的转化率将不变(填“增大”、“减小”、“不变”),再补充 a mol 水蒸气 (H218O),最终容器中C16O和C18O 的物质的量之比为1:a.
(3)己知:C (s)+$\frac{1}{2}$O2(g)═CO (g);△H=-110.5kJ•mo1-1
CO(g)+$\frac{1}{2}$O2(g)═CO2 (g);△H=-283.0kJ•mo1-1
H2 (g)+$\frac{1}{2}$O2 (g)═H2O (g);△H=-241.8kJ•mo1-1
那么,将2.4g 炭完全转化为水煤气,然后再燃烧,整个过程△H=-78.7kJ•mo1-1.
C (s)+H2O(g)?CO (g)+H2 (g);△H=+131.3kJ•mol-1
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中相应的空格.
| 容器编号 | c(H2O)/mol•L-1 | c(CO)/mol•L-1 | c(H2)/mol•L-1 | V正、V逆比较 |
| Ⅰ | 0.06 | 0.60 | 0.10 | V正=V逆 |
| Ⅱ | 0.06 | 0.50 | 0.40 | ? |
| Ⅲ | 0.12 | 0.40 | 0.80 | V正<V逆 |
| Ⅳ | 0.12 | 0.30 | ? | V正=V逆 |
(3)己知:C (s)+$\frac{1}{2}$O2(g)═CO (g);△H=-110.5kJ•mo1-1
CO(g)+$\frac{1}{2}$O2(g)═CO2 (g);△H=-283.0kJ•mo1-1
H2 (g)+$\frac{1}{2}$O2 (g)═H2O (g);△H=-241.8kJ•mo1-1
那么,将2.4g 炭完全转化为水煤气,然后再燃烧,整个过程△H=-78.7kJ•mo1-1.
6. 氮元素可以形成多种氢化物,如NH3、N2H4等.
氮元素可以形成多种氢化物,如NH3、N2H4等.
(1)据报道,2016年中国将发射“天宫二号”空间实验室,并发射“神舟十一号”载人飞船和“天舟一号”货运飞船,与“天宫二号”交会对接.火箭升空需要高能燃料,通常用肼(N2H4)作燃料,N2O4作氧化剂.
已知:N2(g)+O2(g)?2NO(g)△H=+180.7kJ.mol-1
2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ.mol-1
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.0kJ.mol-1
2NO2(g)?N2O4(g)△H=-52.7kJ.mol-1
写出气态肼在气态四氧化二氮中燃烧生成氨气和气态水的热化学方程式:2N2H4(g)+N2O4(g)?3N2(g)+4H2O(g)△H=-1 083.0 kJ•mol-1.
(2)工业上以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为
2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g),该反应的平衡常数和温度关系如下所示:
①该反应的△H<0(填“>”或“<”).
②已知原料气中的氨碳比[$\frac{n(N{H}_{3})}{n(C{O}_{2})}$]为x,CO2的平衡转化率为a,在一定温度和压强下,a与x的关系如图所示.a随着x的增大而增大的原因是增大c(NH3),平衡正向移动,从而提高CO2的转化率.图中A点处,NH3的平衡转化率为42%.
(3)①在氢水加水稀释的过程中,NH3•H2O的电离程度增大(填“增大”、“减小”或“不变”,下同),$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)•c({H}^{+})}$的值不变.
②室温下,amol•L-1的(NH4)2SO4溶液的pH=5,原因是NH4++H2O?NH3•H2O+H+(用离子方程式表示),该反应的平衡常数为$\frac{1{0}^{-5}×(1{0}^{-5}-1{0}^{-9})}{(2a-1{0}^{-5}+1{0}^{-9})}$(用含a的数学表达式表示).
 氮元素可以形成多种氢化物,如NH3、N2H4等.
氮元素可以形成多种氢化物,如NH3、N2H4等.(1)据报道,2016年中国将发射“天宫二号”空间实验室,并发射“神舟十一号”载人飞船和“天舟一号”货运飞船,与“天宫二号”交会对接.火箭升空需要高能燃料,通常用肼(N2H4)作燃料,N2O4作氧化剂.
已知:N2(g)+O2(g)?2NO(g)△H=+180.7kJ.mol-1
2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ.mol-1
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.0kJ.mol-1
2NO2(g)?N2O4(g)△H=-52.7kJ.mol-1
写出气态肼在气态四氧化二氮中燃烧生成氨气和气态水的热化学方程式:2N2H4(g)+N2O4(g)?3N2(g)+4H2O(g)△H=-1 083.0 kJ•mol-1.
(2)工业上以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为
2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g),该反应的平衡常数和温度关系如下所示:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
②已知原料气中的氨碳比[$\frac{n(N{H}_{3})}{n(C{O}_{2})}$]为x,CO2的平衡转化率为a,在一定温度和压强下,a与x的关系如图所示.a随着x的增大而增大的原因是增大c(NH3),平衡正向移动,从而提高CO2的转化率.图中A点处,NH3的平衡转化率为42%.
(3)①在氢水加水稀释的过程中,NH3•H2O的电离程度增大(填“增大”、“减小”或“不变”,下同),$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)•c({H}^{+})}$的值不变.
②室温下,amol•L-1的(NH4)2SO4溶液的pH=5,原因是NH4++H2O?NH3•H2O+H+(用离子方程式表示),该反应的平衡常数为$\frac{1{0}^{-5}×(1{0}^{-5}-1{0}^{-9})}{(2a-1{0}^{-5}+1{0}^{-9})}$(用含a的数学表达式表示).
5.某同学设计aCO2(g)+bH2(g)?cCH3OH(g)+d D(g)(注:D物质未知)来生产甲醇CH3OH,为探究其反应原理进行如下实验,在2L密闭容器内250℃条件下,测得n(CO2)随时间的变化情况如下:
若已知从开始到刚达平衡时用H2表示的平均反应速率是0.05mol/(L•S),平衡时CH3OH的浓度是0.05mol/L,则:
(1)则a与b的关系是?(请写出计算过程,没有计算过程不得分)
(2)请补全反应方程式
1 CO2(g)+3H2(g)?1CH3OH(g)+1H2O(g)
0 172529 172537 172543 172547 172553 172555 172559 172565 172567 172573 172579 172583 172585 172589 172595 172597 172603 172607 172609 172613 172615 172619 172621 172623 172624 172625 172627 172628 172629 172631 172633 172637 172639 172643 172645 172649 172655 172657 172663 172667 172669 172673 172679 172685 172687 172693 172697 172699 172705 172709 172715 172723 203614
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CO2)(mol) | 0.40 | 0.35 | 0.31 | 0.3 | 0.3 | 0.3 |
(1)则a与b的关系是?(请写出计算过程,没有计算过程不得分)
(2)请补全反应方程式
1 CO2(g)+3H2(g)?1CH3OH(g)+1H2O(g)
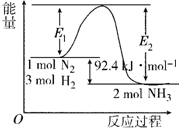 下达到平衡时H2的转化率为33.3%.该温度下的平衡常数K的值为$\frac{100}{27}$.若升高温度,K值减小(填“增大”“减小”或“不变”).
下达到平衡时H2的转化率为33.3%.该温度下的平衡常数K的值为$\frac{100}{27}$.若升高温度,K值减小(填“增大”“减小”或“不变”).