4.绿色能源是指使用过程中不排放或排放极少污染物的能源,下列能源属于绿色能源的是( )
①太阳能 ②木材 ③石油 ④煤 ⑤风能.
①太阳能 ②木材 ③石油 ④煤 ⑤风能.
| A. | ①② | B. | ①⑤ | C. | ②③ | D. | ③④ |
3.有关AgCl沉淀的溶解平衡说法正确的是( )
| A. | AgCl沉淀生成和沉淀溶解不断进行,但速率相等 | |
| B. | AgCl难溶于水,溶液中没有Ag+和Cl- | |
| C. | 在AgCl沉淀溶解平衡体系中加入蒸馏水,AgCl的Ksp增大 | |
| D. | AgCl在相同浓度的CaCl2和NaCl溶液中的溶解度相同 |
1.PCl3可用于半导体生产的外延、扩散工序.有关物质的部分性质如下:
(Ⅰ)制备:
如图是实验室制备PCl3的装置(部分仪器已省略)

(1)仪器乙的名称为冷凝管,其中与自来水进水管连接的编号是b(填“a”或“b”).
(2)实验室常用软锰矿(MnO2)与浓盐酸制备Cl2,反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)碱石灰的作用是碱石灰吸收多余氯气防止污染空气,防止空气中的水蒸气进入影响产品纯度.
(4)向仪器甲中通入干燥的Cl2之前,应先通入一段时间的CO2,其目的是排净装置中的空气,防止空气中的水分和氧气与PCl3反应.
(Ⅱ)提纯:
(5)粗产品中常含有POCl3、PCl5等.加入黄磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到PCl3的纯品.
(Ⅲ)分析:
(6)迅速称取5.5g产品,水解完全后配成500mL溶液,取出25mL,加入过量的0.1mol•L-1碘溶液23mL,充分反应后用0.1mol•L-1Na2S2O3溶液滴定过量的碘,消耗10mLNa2S2O3溶液.
已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6;
假设测定过程中没有发生其他反应.根据上述数据,可计算出该产品中PCl3的质量分数为90.0%.
| 熔点/℃ | 沸点/℃ | 密度/g•mL-1 | 其他 | |
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2PCl3 2P+5Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2PCl5 |
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
如图是实验室制备PCl3的装置(部分仪器已省略)

(1)仪器乙的名称为冷凝管,其中与自来水进水管连接的编号是b(填“a”或“b”).
(2)实验室常用软锰矿(MnO2)与浓盐酸制备Cl2,反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)碱石灰的作用是碱石灰吸收多余氯气防止污染空气,防止空气中的水蒸气进入影响产品纯度.
(4)向仪器甲中通入干燥的Cl2之前,应先通入一段时间的CO2,其目的是排净装置中的空气,防止空气中的水分和氧气与PCl3反应.
(Ⅱ)提纯:
(5)粗产品中常含有POCl3、PCl5等.加入黄磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到PCl3的纯品.
(Ⅲ)分析:
(6)迅速称取5.5g产品,水解完全后配成500mL溶液,取出25mL,加入过量的0.1mol•L-1碘溶液23mL,充分反应后用0.1mol•L-1Na2S2O3溶液滴定过量的碘,消耗10mLNa2S2O3溶液.
已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6;
假设测定过程中没有发生其他反应.根据上述数据,可计算出该产品中PCl3的质量分数为90.0%.
20.A、B、C、D、E是短周期的五种元素,原子序数依次增大,有关信息如下表所示.
填写下列空白.
(1)C元素为N.
(2)由上述两种元素组成的含有非极性键的一种化合物的化学式为H2O2等.
(3)A、B、C、D四种元素原子个数为7:2:1:2的离子化合物的化学式为CH3COONH4.
(4)由上述两种元素组成含有30个电子的阴离子,其钠盐水溶液呈碱性,理由是AlO2-+2H2O?Al(OH)3+OH-(用离子方程式表示).
| 元素 | 部分结构和性质 |
| A | 所有元素中原子半径最小 |
| B | 次外层电子数为最外层电子数的一半 |
| C | 单质由双原子分子构成,分子中有14个电子 |
| D | 地壳中含量最高的元素 |
| E | 最高价氧化物对应的水化物能溶于强酸和强碱 |
(1)C元素为N.
(2)由上述两种元素组成的含有非极性键的一种化合物的化学式为H2O2等.
(3)A、B、C、D四种元素原子个数为7:2:1:2的离子化合物的化学式为CH3COONH4.
(4)由上述两种元素组成含有30个电子的阴离子,其钠盐水溶液呈碱性,理由是AlO2-+2H2O?Al(OH)3+OH-(用离子方程式表示).
19.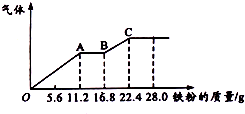 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的最随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的最随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的最随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的最随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )| A. | H2SO4浓度为5mol•L-1 | |
| B. | 第二份溶液中最终溶质为FeSO4 | |
| C. | 每份混合酸中NO3-物质的量为0.2mol | |
| D. | OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
18.下列说法不正确的是( )
| A. | 将pH=4的某酸稀释10倍,测得其pH<5,则该酸为弱酸 | |
| B. | 0.1mol•L-1的NaHCO3溶液中C(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) | |
| C. | 0.1mol•L-1的NaHA溶液pH=5,则溶液:c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-) | |
| D. | pH=4的醋酸与pH=10的氢氧化钠溶液等体积混合,所得溶液pH<7 |
17.咖啡酸结构简式为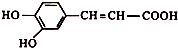 ,有关咖啡酸的说法中不正确的是( )
,有关咖啡酸的说法中不正确的是( )
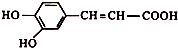 ,有关咖啡酸的说法中不正确的是( )
,有关咖啡酸的说法中不正确的是( )| A. | 咖啡酸分子式是C9H8O4 | |
| B. | 咖啡酸可以发生还原、取代、加聚等反应 | |
| C. | 1mol咖啡酸可以与4molH2发生加成反应 | |
| D. | 1mol咖啡酸最多能消耗3molNaHCO3 |
16.下列各实验选用的实验用品不能都用到的是( )


| A. | 将海带高温灼烧,选用①、②、⑨ | |
| B. | 过滤粗盐水,选用④、⑤、⑦ | |
| C. | 四氯化碳萃取溴水中的溴,选用④、⑥、⑧ | |
| D. | 加热碳酸氢钠固体并检验其产物,选用②、③ |
15.室温下,有pH=3的盐酸、硫酸、醋酸(假设醋酸有1%的电离)三种相同体积的溶液.以下叙述错误的是( )
0 171585 171593 171599 171603 171609 171611 171615 171621 171623 171629 171635 171639 171641 171645 171651 171653 171659 171663 171665 171669 171671 171675 171677 171679 171680 171681 171683 171684 171685 171687 171689 171693 171695 171699 171701 171705 171711 171713 171719 171723 171725 171729 171735 171741 171743 171749 171753 171755 171761 171765 171771 171779 203614
| A. | 溶液的导电性能相同 | |
| B. | 与足量的锌粉反应的起始速率相同 | |
| C. | 与足量的锌粉反应产生氢气的体积比为1:2:100 | |
| D. | 与同浓度氢氧化钠溶液反应,消耗氢氧化钠溶液的体积为1:1:100 |
 ;
; (R1、R2代表烃基或氩原子)
(R1、R2代表烃基或氩原子)
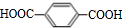 .
. +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O;反应⑦的化学方程式为
+2H2O;反应⑦的化学方程式为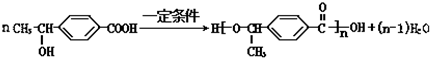 .
.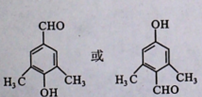 .
.