17.用惰性电极插入KOH溶液中,在两极分别通入CH3OH和O2,有关此电池判断正确的是( )
| A. | 正极反应式:2CH3OH+2H2O-12e-═2CO2↑+12H+ | |
| B. | 放电一段时间后,负极的PH值升高 | |
| C. | 放电一段时间,阳离子向负极移动,阴离子向正极移动 | |
| D. | 该电池在工作时,每消耗32gCH3OH,外电路中通过6mole- |
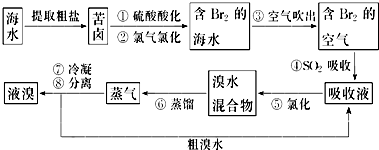
15.黄铁矿石的主要成分为FeS2和少量FeS(假设其他杂质中不含Fe、S元素,且高温下不发生化学变化),是我国大多数硫酸厂制取硫酸的主要原料.某化学兴趣小组对该黄铁矿石进行如下实验探究.将m1g该黄铁矿石的样品放入如图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全.

其反应的化学方程式为:
4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2
4FeS+7O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4SO2
【实验一】:测定硫元素的含量反应结束后,将乙瓶中的溶液进行如下处理:
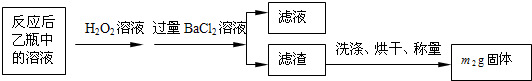
(1)鼓入空气的作用是提供反应需要的氧气,排出装置中生成的二氧化硫被乙装置全部吸收.
(2)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是Na2SO3+H2O2=Na2SO4+H2O(用化学方程式表示).
(3)该黄铁矿石中硫元素的质量分数为$\frac{32{m}_{2}}{233{m}_{1}}$×100%(列出表达式即可).
【实验二】:测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣→②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤→③将滤液稀释至250mL→④取25.00mL稀释液用0.1 000mol/L的酸性KMnO4溶液滴定
(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量偏大(填“偏大”、“偏小”或“无影响”).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有250mL容量瓶.
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
根据所给数据,计算该稀释液中Fe2+的物质的量浓度为c(Fe2+)=0.5000mol/L.

其反应的化学方程式为:
4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2
4FeS+7O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4SO2
【实验一】:测定硫元素的含量反应结束后,将乙瓶中的溶液进行如下处理:

(1)鼓入空气的作用是提供反应需要的氧气,排出装置中生成的二氧化硫被乙装置全部吸收.
(2)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是Na2SO3+H2O2=Na2SO4+H2O(用化学方程式表示).
(3)该黄铁矿石中硫元素的质量分数为$\frac{32{m}_{2}}{233{m}_{1}}$×100%(列出表达式即可).
【实验二】:测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣→②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤→③将滤液稀释至250mL→④取25.00mL稀释液用0.1 000mol/L的酸性KMnO4溶液滴定
(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量偏大(填“偏大”、“偏小”或“无影响”).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有250mL容量瓶.
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 消耗KMnO4溶液体积/mL | 25.00 | 25.03 | 20.00 | 24.97 |
12.在下列各溶液中,离子一定能大量共存的是( )
| A. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- | |
| B. | 碱性溶液中:K+、Mg2+、S2-、ClO- | |
| C. | 加入铝粉有气泡产生的溶液中:Na+、NH4+、Fe2+、NO3- | |
| D. | 在AlCl3溶液中:K+、Na+、SiO32-、SO42- |
11.如图所示的装置,C.D.E.F.X.Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色.则以下说法正确的是( )

0 171126 171134 171140 171144 171150 171152 171156 171162 171164 171170 171176 171180 171182 171186 171192 171194 171200 171204 171206 171210 171212 171216 171218 171220 171221 171222 171224 171225 171226 171228 171230 171234 171236 171240 171242 171246 171252 171254 171260 171264 171266 171270 171276 171282 171284 171290 171294 171296 171302 171306 171312 171320 203614

| A. | 电源B极是正极 | |
| B. | 欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 | |
| C. | 甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1:2:2:2 | |
| D. | 装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带负电荷 |
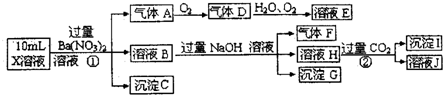
 将全部由短周期元素组成的化合物X加热分解,可得A、B、C、D、E和H2O六种产物,其中A、B、C都是中学化学中常见的氧化物,气体D是单质E所含元素的氢化物.
将全部由短周期元素组成的化合物X加热分解,可得A、B、C、D、E和H2O六种产物,其中A、B、C都是中学化学中常见的氧化物,气体D是单质E所含元素的氢化物.