7.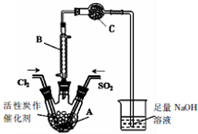 某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.
某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.
(1)若用浓盐酸与二氧化锰为原料制取Cl2,反应的化学方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)C仪器装的药品是无水CaCl2,其作用是防止水蒸气进入A装置(引起SO2Cl2水解);
(3)为了便于混合物的分离且提高反应物的转化率,A装置的反应条件最好选择
a.冰水浴 b.常温 c.加热至69.1℃
(4)如果通入的Cl2或SO2含有水蒸气,氯气和二氧化硫可能发生反应的化学方程式为SO2+Cl2+2H2O=H2SO4+2HCl;
(5)实验时选通入干燥的Cl2将A装置中的空气赶走,再缓慢通入干燥的SO2,即发生反应.充分反应后,继续通入Cl2使装置中的SO2进入烧杯中被吸收,分离产物后,向获得的SO2Cl2中加水,出现白雾,振荡、静置得到无色溶液W.
①经分析SO2Cl2与H2O反应性于非氧化还原反应,写出该反应的化学方程式SO2Cl2+2H2O=H2SO4+2HCl;
②无色溶液W中的阴离子除含少量OH-外,还含有其它两种阴离子,如需检验溶液W中这两种阴离子,则其检出第一种离子的检验方法是取少量W溶液于试管中,加入过量Ba(NO3)2溶液,有不溶于稀硝酸的白色沉淀产生,说明溶液中含有SO42-;
③反应完成后,在W溶液、烧杯中分别滴加过量的BaCl2溶液,均出现白色沉淀,此沉淀不溶于稀盐酸,经过滤、洗涤、干燥、称量得到的固体质量分别为Xg、Yg,则SO2+Cl2?SO2Cl2反应中,SO2的转化率为$\frac{X}{X+Y}$×100%(用含X、Y的代数式表示).
 某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.
某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.(1)若用浓盐酸与二氧化锰为原料制取Cl2,反应的化学方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)C仪器装的药品是无水CaCl2,其作用是防止水蒸气进入A装置(引起SO2Cl2水解);
(3)为了便于混合物的分离且提高反应物的转化率,A装置的反应条件最好选择
a.冰水浴 b.常温 c.加热至69.1℃
(4)如果通入的Cl2或SO2含有水蒸气,氯气和二氧化硫可能发生反应的化学方程式为SO2+Cl2+2H2O=H2SO4+2HCl;
| SO2Cl2 | Cl2 | SO2 | |
| 熔点 | -54.1 | -101 | -72.4 |
| 沸点 | 69.1 | -34.6 | -10 |
| 性质 | 遇水发生剧烈水解 |
①经分析SO2Cl2与H2O反应性于非氧化还原反应,写出该反应的化学方程式SO2Cl2+2H2O=H2SO4+2HCl;
②无色溶液W中的阴离子除含少量OH-外,还含有其它两种阴离子,如需检验溶液W中这两种阴离子,则其检出第一种离子的检验方法是取少量W溶液于试管中,加入过量Ba(NO3)2溶液,有不溶于稀硝酸的白色沉淀产生,说明溶液中含有SO42-;
③反应完成后,在W溶液、烧杯中分别滴加过量的BaCl2溶液,均出现白色沉淀,此沉淀不溶于稀盐酸,经过滤、洗涤、干燥、称量得到的固体质量分别为Xg、Yg,则SO2+Cl2?SO2Cl2反应中,SO2的转化率为$\frac{X}{X+Y}$×100%(用含X、Y的代数式表示).
5.资料显示:
a.Na2S2O3、BaS2O3、BaS均易溶于水.
b.SO2、Na2S、Na2CO3反应可生成Na2S2O3.
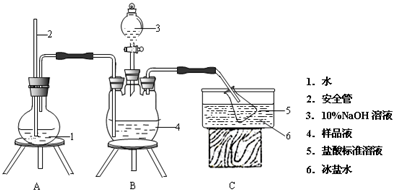
某化学小组据此进行了制备硫代硫酸钠(Na2S2O3)的探究,实验制备装置如图所示(省略夹持装置):

回答问题:
(1)仪器a的名称是分液漏斗.
(2)装置A中发生反应的化学方程式是Na2SO3+H2SO4=Na2SO4+SO2↑+H2O.
(3)装置B的作用之一是观察SO2的生成速率.
①B中最好盛装的液体是c.
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
②如使SO2缓慢进入烧瓶C,正确的操作是控制分液漏斗的活塞,使浓硫酸缓慢滴入A中.
(4)在装置C中生成Na2S2O3.
①完成反应方程式:4SO2+2Na2S+1Na2CO3=3Na2S2O3+CO2
②反应开始先使A中发生反应一会儿,再使C中反应发生,其原因是A中反应一会生成二氧化硫,C中才能反应.
③结束反应后,取C中溶液,经蒸发、结晶、过滤、洗涤、干燥、得到Na2S2O3•5H2O.
(5)完成对所得产品的检测的实验:
a.Na2S2O3、BaS2O3、BaS均易溶于水.
b.SO2、Na2S、Na2CO3反应可生成Na2S2O3.
某化学小组据此进行了制备硫代硫酸钠(Na2S2O3)的探究,实验制备装置如图所示(省略夹持装置):

回答问题:
(1)仪器a的名称是分液漏斗.
(2)装置A中发生反应的化学方程式是Na2SO3+H2SO4=Na2SO4+SO2↑+H2O.
(3)装置B的作用之一是观察SO2的生成速率.
①B中最好盛装的液体是c.
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
②如使SO2缓慢进入烧瓶C,正确的操作是控制分液漏斗的活塞,使浓硫酸缓慢滴入A中.
(4)在装置C中生成Na2S2O3.
①完成反应方程式:4SO2+2Na2S+1Na2CO3=3Na2S2O3+CO2
②反应开始先使A中发生反应一会儿,再使C中反应发生,其原因是A中反应一会生成二氧化硫,C中才能反应.
③结束反应后,取C中溶液,经蒸发、结晶、过滤、洗涤、干燥、得到Na2S2O3•5H2O.
(5)完成对所得产品的检测的实验:
| 推测 | 操作和现象 | 结论 |
| 杂质中的正盐成分可能有: Na2S Na2CO3 Na2SO3 Na2SO4 | ①取Wg产品配成稀溶液; ②向溶液中滴加过量BaCl2溶液,有白色沉淀生成,过滤,得沉淀和滤液; ③向沉淀中加入过量盐酸,沉淀完全溶解,并有刺激性气味的气体产生. ④向滤液滴加2滴淀粉溶液,再逐滴加0.100 0mol•L-1碘的标准溶液,至溶液呈紫色不再褪去,消耗碘的标准溶液体积为18.10mL. | 产品杂质中: 一定含有Na2SO3, 可能含有Na2S、Na2CO3, 一定不含有Na2SO4. 操作④发生的反应是: 2S2O${\;}_{3}^{2-}$+I2═S4O${\;}_{6}^{2-}$+2I- 产品纯度:$\frac{9}{w}$×100%. |
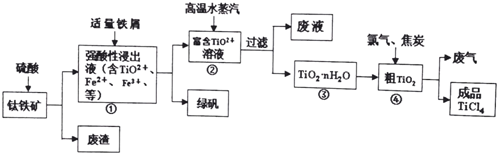
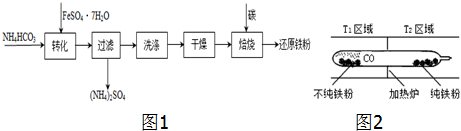
3.FeSO4•7H2O广泛用于医药和工业领域,实验室制备FeSO4•7H2O的流程如下:

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是除去废铁屑表面的油污.
(2)最后得到的绿矾晶体用少量冰水洗涤,其目的:①除去晶体表面附着的硫酸等杂质;
②降低FeSO4在水中的溶解度,减少FeSO4•7H2O的损耗.
(3)FeSO4•7H2O是某些补血剂的主要成分,实验室用KMnO4溶液通过氧化还原滴定测
定某补血剂(1.500g)中铁元素的含量.
①配制100mL 1.200×10 -2mol•L-1的KMnO4溶液时,将溶解后的溶液转移至容 量瓶中的操作方法是用玻璃棒引流,玻璃棒底部要在容量瓶的刻度线以下且玻璃棒不能碰到容量瓶口;
②实验中的KMnO4溶液需要酸化,可用于酸化的酸是c.
a.稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
KMnO4溶液应盛装在酸式滴定管中.滴定到终点时的现象为滴入最后一滴KMnO4溶液,恰好变为紫红色,且半分钟内不退色.滴定完毕,三次实验记录KMnO4标准溶液的读数如下.
该补血剂中铁元素的质量分数为3.36%.
(4)某实验小组用久置的FeSO4溶液和NaOH溶液制备Fe(OH)2,实验后没有得到预期的白色沉淀,于是采用下列试剂(已煮沸除氧)和装置进行实验:

实验开始打开止水夹C,目的是排除装置中的空气,防止氢氧化亚铁被氧化为氢氧化铁.一段时间后,关闭止水夹C,B中观察到的现象是液面上升出现白色沉淀.B中发生反应的离子方程式是Fe2++2OH-=Fe(OH)2↓.
0 171015 171023 171029 171033 171039 171041 171045 171051 171053 171059 171065 171069 171071 171075 171081 171083 171089 171093 171095 171099 171101 171105 171107 171109 171110 171111 171113 171114 171115 171117 171119 171123 171125 171129 171131 171135 171141 171143 171149 171153 171155 171159 171165 171171 171173 171179 171183 171185 171191 171195 171201 171209 203614

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是除去废铁屑表面的油污.
(2)最后得到的绿矾晶体用少量冰水洗涤,其目的:①除去晶体表面附着的硫酸等杂质;
②降低FeSO4在水中的溶解度,减少FeSO4•7H2O的损耗.
(3)FeSO4•7H2O是某些补血剂的主要成分,实验室用KMnO4溶液通过氧化还原滴定测
定某补血剂(1.500g)中铁元素的含量.
①配制100mL 1.200×10 -2mol•L-1的KMnO4溶液时,将溶解后的溶液转移至容 量瓶中的操作方法是用玻璃棒引流,玻璃棒底部要在容量瓶的刻度线以下且玻璃棒不能碰到容量瓶口;
②实验中的KMnO4溶液需要酸化,可用于酸化的酸是c.
a.稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
KMnO4溶液应盛装在酸式滴定管中.滴定到终点时的现象为滴入最后一滴KMnO4溶液,恰好变为紫红色,且半分钟内不退色.滴定完毕,三次实验记录KMnO4标准溶液的读数如下.
| 滴定次数实验数据 | 1 | 2 | 3 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 |
| V(KMnO4)/mL(初读数) | 0.00 | 0.20 | 0.00 |
| V(KMnO4)/mL(终读数) | 15.85 | 15.22 | 14.98 |
(4)某实验小组用久置的FeSO4溶液和NaOH溶液制备Fe(OH)2,实验后没有得到预期的白色沉淀,于是采用下列试剂(已煮沸除氧)和装置进行实验:

实验开始打开止水夹C,目的是排除装置中的空气,防止氢氧化亚铁被氧化为氢氧化铁.一段时间后,关闭止水夹C,B中观察到的现象是液面上升出现白色沉淀.B中发生反应的离子方程式是Fe2++2OH-=Fe(OH)2↓.

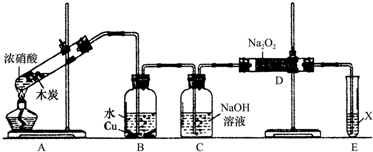
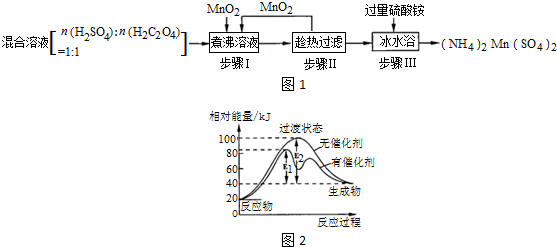
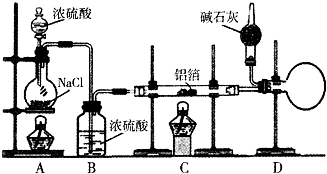 无水氯化铝是有机化工常用的催化剂,氯化铝178℃时升华,极易潮解,遇水发热并产生白色烟雾.氯化铝还易溶于乙醇、氯仿和四氯化碳.实验室可用反应2Al+6HCl(g)$\frac{\underline{\;\;△\;\;}}{\;}$2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置:
无水氯化铝是有机化工常用的催化剂,氯化铝178℃时升华,极易潮解,遇水发热并产生白色烟雾.氯化铝还易溶于乙醇、氯仿和四氯化碳.实验室可用反应2Al+6HCl(g)$\frac{\underline{\;\;△\;\;}}{\;}$2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置: