19.A、B、C、D、E为原子序数依次增大的短周期元素,其中只有一种是金属元素.A、D元素原子最外层电子数相同,且A和D可形成离子化合物,C2-和D+具有相同的电子数,E元素的最高正化合价与最低负化合价之和为2.由这些元素组成的物质,其组成和结构信息如下表:
请用化学用语回答下列问题:
(1)D+的结构示意图为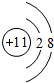 ;
;
(2)C、D、E的氢化物按熔点由高到低排列的顺序为NaH>H2O>PH3;
(3)乙属于极性分子(填“极性”或“非极性”),丁的电子式为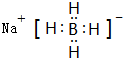 ,
,
(4)将少量甲投入到AlCl3溶液中反应的离子方程式为6Na2O2+4Al3+6H2O=4Al(OH)3↓+3O2↑+12Na+;
(5)氮化硼晶体的熔点要比丙晶体高,其原因是磷原子半径比氮原子大,N-B共价键键长比B-P小,则N-B键能大.
| 物质 | 组成和结构信息 |
| 甲 | 含有非极性共价键的常见二元离子化合物 |
| 乙 | 含有极性键和非极性键的18e-分子 |
| 丙 | 化学组成为BE,熔点高,可作超硬耐磨涂层材料 |
| 丁 | 化学组成为DBA4的离子化合物 |
(1)D+的结构示意图为
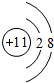 ;
;(2)C、D、E的氢化物按熔点由高到低排列的顺序为NaH>H2O>PH3;
(3)乙属于极性分子(填“极性”或“非极性”),丁的电子式为
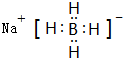 ,
,(4)将少量甲投入到AlCl3溶液中反应的离子方程式为6Na2O2+4Al3+6H2O=4Al(OH)3↓+3O2↑+12Na+;
(5)氮化硼晶体的熔点要比丙晶体高,其原因是磷原子半径比氮原子大,N-B共价键键长比B-P小,则N-B键能大.
18.在化学学习中使用数轴的表示方法可起到直观、形象的效果,下列表达中不正确的是( )
| A. | 常温下溶液的pH与酸碱性的关系: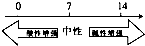 | |
| B. | 硫的化合物中化合价与其氧化性、还原性的关系: | |
| C. | Fe在Cl2中的燃烧产物: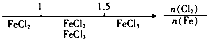 | |
| D. | 氨水与SO2反应后溶液中的铵盐: |
16.某种烃或其一种同分异构体的一氯代物只有一种结构,则该烃的分子式不可能是( )
| A. | C2H6 | B. | C4H10 | C. | C5H12 | D. | C6H6 |
15.下列关于指定粒子构成的叙述中,不正确的是( )
0 170923 170931 170937 170941 170947 170949 170953 170959 170961 170967 170973 170977 170979 170983 170989 170991 170997 171001 171003 171007 171009 171013 171015 171017 171018 171019 171021 171022 171023 171025 171027 171031 171033 171037 171039 171043 171049 171051 171057 171061 171063 171067 171073 171079 171081 171087 171091 171093 171099 171103 171109 171117 203614
| A. | 37Cl与39K具有相同的中子数 | |
| B. | 第114号元素的一种核素${\;}_{114}^{298}X$与${\;}_{82}^{207}Pb$具有相同的最外层电子数 | |
| C. | O22-与S2-具有相同的质子数和电子数 | |
| D. | H3O+与OH-具有相同的质子数和电子数 |
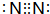 ,物质甲分子的结构式
,物质甲分子的结构式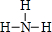 .
. .
.
 A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,它们之间的转化关系如图所示((图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).
A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,它们之间的转化关系如图所示((图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).
 根据图中A、B两种固体物质的溶解度曲线,回答下列问题:
根据图中A、B两种固体物质的溶解度曲线,回答下列问题: