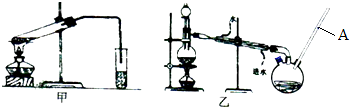
9.某溶液中,除水电离出的H+、OH-之外仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种,这4种离子的物质的量均为0.1mol.若向该溶液中加入足量稀硫酸,无沉淀生成但有无色气泡产生.下列说法错误的是( )
| A. | 该溶液中一定不含Ba2+ | |
| B. | 该溶液中一定含Na+ | |
| C. | 无色气体在标准状况下的体积约为2.24L | |
| D. | 若向该溶液中加入足量NaOH溶液,滤出沉淀,洗净灼烧后最多能得8.0g固体 |
8.分子组成为C4H9OH并能发生催化氧化反应但不能得到醛的有机化合物有( )
| A. | 4种 | B. | 3种 | C. | 2种 | D. | 1种 |
6.开发新型储氢材料是氢能利用的重要研究方向.
Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
(1)基态Ti3+的未成对电子数有1个.
(2)LiBH4由Li+和BH4-构成,LiBH4中不存在的作用力有C(填标号).
A.离子键 B.共价键 C.金属键 D.配位键
(3)Li、B、H元素的电负性由大到小排列顺序为H>B>Li.
(4)分子X可以通过氢键形成“笼状结构”而成为潜在的储氢材料.X一定不是BC(填标号).
A.H2O B.CH4 C.HF D.CO(NH2)2
(5)钾、镁、氟形成的某化合物的晶体结构为K+在立方晶胞的中心,Mg2+在晶胞的8个顶角,F-处于晶胞的棱边中心.由钾、镁、氟形成的该化合物的化学式为KMgF3,每个K+与12个F-配位.
(6)判断含氧酸酸性强弱的一条经验规律是含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强.如下表所示:含氧酸酸性强弱与非羟基氧原子数的关系
亚磷酸H3PO3和亚砷酸H3AsO3分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性.由此可推出H3AsO3结构式为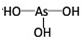 .H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:
.H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:
①H3PO3+2NaOH=Na2HPO3+2H2O,
②H3AsO3+3NaOH=Na3AsO3+3H2O.
Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
(1)基态Ti3+的未成对电子数有1个.
(2)LiBH4由Li+和BH4-构成,LiBH4中不存在的作用力有C(填标号).
A.离子键 B.共价键 C.金属键 D.配位键
(3)Li、B、H元素的电负性由大到小排列顺序为H>B>Li.
(4)分子X可以通过氢键形成“笼状结构”而成为潜在的储氢材料.X一定不是BC(填标号).
A.H2O B.CH4 C.HF D.CO(NH2)2
(5)钾、镁、氟形成的某化合物的晶体结构为K+在立方晶胞的中心,Mg2+在晶胞的8个顶角,F-处于晶胞的棱边中心.由钾、镁、氟形成的该化合物的化学式为KMgF3,每个K+与12个F-配位.
(6)判断含氧酸酸性强弱的一条经验规律是含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强.如下表所示:含氧酸酸性强弱与非羟基氧原子数的关系
| 次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
| 含氧酸 | Cl-OH | 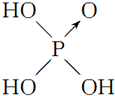 |  | 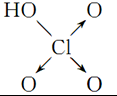 |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
 .H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:
.H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:①H3PO3+2NaOH=Na2HPO3+2H2O,
②H3AsO3+3NaOH=Na3AsO3+3H2O.
1.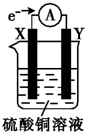 将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示).据此判断下列说法正确的是( )
将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示).据此判断下列说法正确的是( )
 将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示).据此判断下列说法正确的是( )
将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示).据此判断下列说法正确的是( )| A. | 外电路中电流方向为X→Y | |
| B. | 若电极材料分别为锌片和铜片,则Y为锌片 | |
| C. | X极上发生还原反应 | |
| D. | 若电极材料都是金属,则金属活动性:X>Y |
20.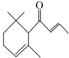 一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构简式如图.有关该化合物的下列说法不正确的是( )
一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构简式如图.有关该化合物的下列说法不正确的是( )
0 170910 170918 170924 170928 170934 170936 170940 170946 170948 170954 170960 170964 170966 170970 170976 170978 170984 170988 170990 170994 170996 171000 171002 171004 171005 171006 171008 171009 171010 171012 171014 171018 171020 171024 171026 171030 171036 171038 171044 171048 171050 171054 171060 171066 171068 171074 171078 171080 171086 171090 171096 171104 203614
 一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构简式如图.有关该化合物的下列说法不正确的是( )
一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构简式如图.有关该化合物的下列说法不正确的是( )| A. | 分子式为C13H20O | |
| B. | 该化合物可发生加聚反应 | |
| C. | 1 mol该化合物完全燃烧消耗18molO2 | |
| D. | 该物质能使溴水和酸性KMnO4溶液褪色 |
 .
.