8.
(1)电离平衡常数是衡量弱电解质电离程度强弱的量.上表中给出几种弱电解质的电离平衡常数,从中可以判断:在相同温度下,同浓度的三种酸溶液的导电能力由大到小的顺序为CH3COOH>H2CO3>HCN.
(2)盐类水解程度的强弱同样与弱电解质的电离程度有一定联系,结合表中数据回答下列问题:
①25℃时,有等浓度的a.NaCN溶液、b.Na2CO3溶液、c.CH3COONa溶液,三种溶液的pH由大到小的顺序为b>a>c.(填溶液前序号)
②浓度相同的NaCN溶液与CH3COOK溶液相比,c(Na+)-c(CN-)>c(K+)-c(CH3COO-).(填“>”、“<”或“=”)
③将等体积等物质的量浓度的盐酸和氨水混合后,溶液呈酸性(填“酸”、“碱”或“中”),用离子方程式表示原因NH4++H2O?NH3•H2O+H+
④室温下,若将0.1mol•L-1盐酸滴入20mL 0.1mol•L-1氨水中,溶液pH随加入盐酸体积的变化曲线如下图所示.b点所示溶液中的溶质是NH3•H2O、NH4Cl
⑤NH4HCO3溶液呈碱性(填“酸”、“碱”或“中”)
(3)结合表中数据,向NaCN溶液中通入少量CO2,所发生反应的化学方程式NaCN+H2O+CO2=HCN+NaHCO3.

| 化学式 | NH3•H2O | HCN | CH3COOH | H2CO3 |
| 电离平衡常数(25℃) | Kb=1.77×10-5 | Ka=4.93×10-10 | Ka=1.76×10-5 | Ka1=4.30×10-7 Ka2=5.61×10-11 |
(2)盐类水解程度的强弱同样与弱电解质的电离程度有一定联系,结合表中数据回答下列问题:
①25℃时,有等浓度的a.NaCN溶液、b.Na2CO3溶液、c.CH3COONa溶液,三种溶液的pH由大到小的顺序为b>a>c.(填溶液前序号)
②浓度相同的NaCN溶液与CH3COOK溶液相比,c(Na+)-c(CN-)>c(K+)-c(CH3COO-).(填“>”、“<”或“=”)
③将等体积等物质的量浓度的盐酸和氨水混合后,溶液呈酸性(填“酸”、“碱”或“中”),用离子方程式表示原因NH4++H2O?NH3•H2O+H+
④室温下,若将0.1mol•L-1盐酸滴入20mL 0.1mol•L-1氨水中,溶液pH随加入盐酸体积的变化曲线如下图所示.b点所示溶液中的溶质是NH3•H2O、NH4Cl
⑤NH4HCO3溶液呈碱性(填“酸”、“碱”或“中”)
(3)结合表中数据,向NaCN溶液中通入少量CO2,所发生反应的化学方程式NaCN+H2O+CO2=HCN+NaHCO3.
1.常温常压下,24ml氢气和氧气的混合气体,点燃反应后再恢复到原来温度和压强.剩余气体体积为3ml,则原混合气体中氢气与氧气的分子个数比可能是( )
| A. | 1:16 | B. | 16:1 | C. | 17:7 | D. | 5:7 |
20.将一定体积密度为1.32g/cm3的硫酸溶液逐滴滴入到BaCl2溶液中,直到沉淀恰好完全为止.已知反应后所得溶液的质量等于原BaCl2溶液的质量,则原硫酸溶液浓度为( )
| A. | 23.9% | B. | 11.0% | C. | 13.5mol/L | D. | 5.67mol/L |
19.下列物质分类合理的是( )
0 170865 170873 170879 170883 170889 170891 170895 170901 170903 170909 170915 170919 170921 170925 170931 170933 170939 170943 170945 170949 170951 170955 170957 170959 170960 170961 170963 170964 170965 170967 170969 170973 170975 170979 170981 170985 170991 170993 170999 171003 171005 171009 171015 171021 171023 171029 171033 171035 171041 171045 171051 171059 203614
| A. | 氧化物:CO2NO SO2H2O | |
| B. | 碱:NaOH KOH Ba(OH)2Na2CO3 | |
| C. | 铵盐:NH4Cl NH4NO3(NH4)2SO4NH3-H2O | |
| D. | 碱性氧化物:Na2O CaO Mn2O7 Al2O3 |
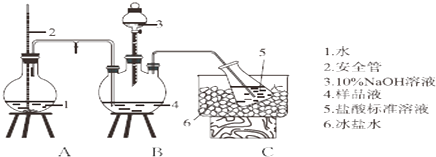
 图中表示A~E五种物质的转化关系.若将它们灼烧,火焰都呈黄色;A能跟水起剧烈反应,D常用作潜水艇里的氧气来源.
图中表示A~E五种物质的转化关系.若将它们灼烧,火焰都呈黄色;A能跟水起剧烈反应,D常用作潜水艇里的氧气来源. .
.
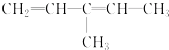 该烃系统命名为:3-甲基-1,3-戊二烯
该烃系统命名为:3-甲基-1,3-戊二烯 .
. A、B、C是中学化学中常见的单质,常温下甲、乙两种化合物分别是黑色固体和无色液体,这些化合物和单质之间有如图所示关系.据此判断:
A、B、C是中学化学中常见的单质,常温下甲、乙两种化合物分别是黑色固体和无色液体,这些化合物和单质之间有如图所示关系.据此判断: