题目内容
19.下列物质分类合理的是( )| A. | 氧化物:CO2NO SO2H2O | |
| B. | 碱:NaOH KOH Ba(OH)2Na2CO3 | |
| C. | 铵盐:NH4Cl NH4NO3(NH4)2SO4NH3-H2O | |
| D. | 碱性氧化物:Na2O CaO Mn2O7 Al2O3 |
分析 氧化物是由两种元素组成并且一种元素是氧元素的化合物;
电离产生阴离子都是氢氧根离子的化合物属于碱;
铵盐是指电离产生铵根离子的盐;
与酸反应生成产物都只有盐和水的氧化物,属于碱性氧化物.
解答 解:A.CO2NO SO2 H2O都是由两种元素组成并且一种元素是氧元素的化合物,都是氧化物,故A正确;
B.Na2CO3属于盐,故B错误;
C.NH3•H2O属于碱,故C错误;
D.Mn2O7 是酸性氧化物,Al2O3是两性氧化物,故D错误;
故选:A.
点评 本题考查了物质的分类,熟悉酸、碱、盐、氧化物、碱性氧化物的概念是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.已知一定条件下断裂或生成某些化学键的能量关系如下表:
对于反应:H2+I2=2HI,下列说法正确的是( )
| 断裂或生成的化学键 | 能量数据 |
| 断裂1mol H2分子中的化学键 | 吸收能量436kJ |
| 断裂1mol I2分子中的化学键 | 吸收能量151kJ |
| 形成1mol HI分子中的化学键 | 释放能量299kJ |
| A. | 该反应为放热反应 | |
| B. | 该反应中反应物总能量低于生成物总能量 | |
| C. | HI分子中的化学键比H2分子中的化学键更牢固 | |
| D. | 无法判断 |
7.有关化学用语正确的是( )
| A. | 乙酸的分子式CH3COOH | |
| B. | 乙烯的结构简式CH2CH2 | |
| C. | 丙烷的球棍模型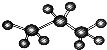 | |
| D. | 乙醇的官能团是-OH,带一个单位负电荷 |
8.短周期元素X、Y、Z、W、Q在元素周期表中相对位置如图所示.下列说法正确的是( )
| X | Y | ||||
| Z | W | Q | |||
| A. | 工业上通过电解熔融Z2Y3制备单质Z | |
| B. | 元素Z的氧化物只能与强酸反应 | |
| C. | 原子半径的大小顺序为:rX<rY | |
| D. | 元素W的最高价氧化物对应的水化物的酸性比Q的强 |
9.下列说法正确的是( )
| A. | 第三周期非金属元素的含氧酸的酸性从左到右依次增强 | |
| B. | HF、HCl、HBr、HI的热稳定性和还原性从上到下依次减弱 | |
| C. | 在ⅥA族元素的氢化物(H2R)中,沸点最高的一定是无毒的 | |
| D. | 同一主族的元素,原子半径越大,其单质的熔点也一定越高 |
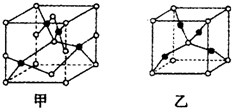 ,化合物的化学式,甲为CuO,乙为Cu2O;高温时,甲易转化为乙的原因为Cu2O中Cu原子d轨道为全满状态,比较稳定.
,化合物的化学式,甲为CuO,乙为Cu2O;高温时,甲易转化为乙的原因为Cu2O中Cu原子d轨道为全满状态,比较稳定.