14.以下事实不能用化学平衡移动原理解释的是( )
| A. | 夏天打开啤酒瓶,有大量气泡逸出 | |
| B. | 对于反应I2(g)+H2(g)?2HI(g)达到平衡后,增大压强气体颜色加深 | |
| C. | 紫色CoCl2溶液,加热溶液颜色变为蓝色,用冰水冷却溶液颜色变为粉红色 | |
| D. | 工业合成氨(N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol)选择高压条件 |
13.下列实验操作或描述中正确的是( )
| A. | 用托盘天平称取5.85g氯化钠固体 | |
| B. | 提取碘水中的碘单质时,可选用酒精作萃取剂 | |
| C. | 观察钾元素焰色反应的操作是:将铂丝在稀盐酸中洗涤后直接蘸取固体氯化钾,置于酒精灯火焰上进行灼烧,根据火焰是否显紫色来确定 | |
| D. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
12.下列叙述不正确的是( )
| A. | 分散质粒子的半径在10-9m~10-7m之间的分散系叫做胶体 | |
| B. | 少量金属钠可保存在煤油中 | |
| C. | CO2水溶液能导电,因此CO2是电解质 | |
| D. | 汤姆生、卢瑟福、玻尔等科学家对原子结构模型的提出作出了很大贡献 |
10.下列事实中不能用勒夏特列原理解释的是( )
| A. | 在溴水中存在如下平衡:Br2+H2O?HBr+HBrO,当加入NaOH溶液后颜色变浅 | |
| B. | 对2NO2(g)?N2O4(g) 平衡体系,增加压强使颜色变浅 | |
| C. | 反应CO+NO2?CO2+NO△H<0升高温度使平衡向逆方向移动 | |
| D. | 向双氧水溶液中滴入FeCl3 溶液后,产生气泡速率加快 |
9.已知某温度时,2SO2(g)+O2(g)?2SO3(g)△H=-Q kJ•mol-1,在相同条件下,向一密闭容器中通2mol SO2和1mol O2,达到平衡时放出热量为Q1;向另一体积相同密闭容器中通1mol SO2和0.5mol O2,达到平衡时放出热量为Q2.则下列关系正确的是( )
| A. | 2 Q2=Q1 | B. | 2 Q2>Q1 | C. | 2 Q2<Q1<Q | D. | Q=Q1>Q2 |
8.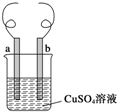 用铁丝(电极 a)、铜丝(电极 b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )
用铁丝(电极 a)、铜丝(电极 b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )
 用铁丝(电极 a)、铜丝(电极 b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )
用铁丝(电极 a)、铜丝(电极 b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )| A. | 构成原电池时 b 极反应为:Cu-2e-═Cu2+ | |
| B. | 构成电解池时 a 极质量一定减少 | |
| C. | 构成的原电池或电解池工作后都能产生大量气体 | |
| D. | 构成电解池时 b 极质量可能减少也可能增加 |
7.已知H2(g)+I2(g)?2HI(g)△H<0有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI 0.2mol,相同温度下分别达到平衡.欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
| A. | 甲温度不变、乙降低温度 | |
| B. | 甲中加入0.1mol He,乙不改变 | |
| C. | 甲增加0.1mol H2,乙增加0.1mol I2(g) | |
| D. | 甲降低温度,乙温度不变 |
5.下列物质属于弱电解质的是( )
0 170783 170791 170797 170801 170807 170809 170813 170819 170821 170827 170833 170837 170839 170843 170849 170851 170857 170861 170863 170867 170869 170873 170875 170877 170878 170879 170881 170882 170883 170885 170887 170891 170893 170897 170899 170903 170909 170911 170917 170921 170923 170927 170933 170939 170941 170947 170951 170953 170959 170963 170969 170977 203614
| A. | Cl2 | B. | CO2 | C. | NH3•H2O | D. | AgCl |