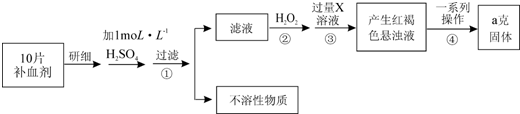
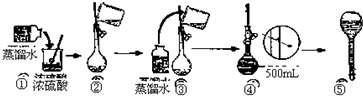
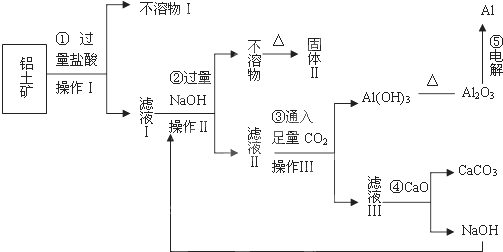
15.反应4NH3+5O2?4NO+6H2O在一定体积的密闭容器中进行,30s后NO的物质的量浓度增加了3mol/L,则下列反应速率正确的是( )
| A. | v(NO)=0.01mol•(L•s)-1 | B. | v(NO)=0.02mol•(L•s)-1 | ||
| C. | v(NH3)=0.1mol•(L•s)-1 | D. | v(NH3)=0.2mol•(L•s)-1 |
13.下列说法正确的是( )
| A. | 矿泉水中含有多种微量元素,经常饮用有益身体健康 | |
| B. | 营养强化剂吃的越多越好 | |
| C. | 合理选择饮食,正确使用药物是人体健康的保证 | |
| D. | 大部分药物都无毒副作用,都是非处方药 |
12.下列离子的检验不能达到预期目的是( )
| A. | 向待测液里加入NaOH溶液,产生红褐色沉淀,则待测液中肯定含有Fe3+ | |
| B. | 向待测液里加入BaCl2溶液,若产生白色沉淀,再加入过量稀硝酸白色沉淀不溶解,则表明待测液中肯定含有SO42- | |
| C. | 向待测液里加入过量硝酸无现象,再加入硝酸银溶液,若无沉淀生成,则表明待测液中肯定不含Cl- | |
| D. | 向待测液里加入CaCl2溶液,不产生白色沉淀,加入稀盐酸产生无色无味气体,该气体通入澄清石灰水中,溶液变浑浊,则表明待测液中肯定含HCO3- |
11.下列化学反应的离子方程式正确的是( )
0 170698 170706 170712 170716 170722 170724 170728 170734 170736 170742 170748 170752 170754 170758 170764 170766 170772 170776 170778 170782 170784 170788 170790 170792 170793 170794 170796 170797 170798 170800 170802 170806 170808 170812 170814 170818 170824 170826 170832 170836 170838 170842 170848 170854 170856 170862 170866 170868 170874 170878 170884 170892 203614
| A. | 将二氧化碳气体通入澄清石灰水中:2OH-+CO2=CO32-+H2O | |
| B. | 往碳酸镁中滴加稀盐酸:CO32-+2H+=CO2↑+H2O | |
| C. | 少量金属钠放入冷水中:Na+2H2O=Na++2OH-+H2↑ | |
| D. | 用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |

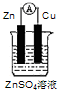

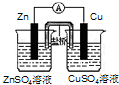

 利用反应2Fe3++Fe═3Fe2+,设计原电池如图所示.
利用反应2Fe3++Fe═3Fe2+,设计原电池如图所示.