20.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:Ar(填具体元素符号,下同),原子结构示意图为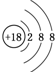 .元素⑩名称为溴在周期表中的位置第四周期第ⅦA族.
.元素⑩名称为溴在周期表中的位置第四周期第ⅦA族.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是: .
.
(3)用电子式表示元素④与⑥的化合物的形成过程: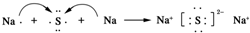 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.
(4)表示①与⑦的化合物的电子式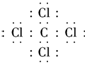 ,该化合物是由极性(填“极性”、“非极性”)键形成的.
,该化合物是由极性(填“极性”、“非极性”)键形成的.
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是S2->Cl->O2-.
(6)元素③的氢化物的结构式为H-O-H;该氢化物常温下和元素⑦的单质反应的化学方程式为Cl2+H2O═HClO+HCl.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .元素⑩名称为溴在周期表中的位置第四周期第ⅦA族.
.元素⑩名称为溴在周期表中的位置第四周期第ⅦA族.(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是:
 .
.(3)用电子式表示元素④与⑥的化合物的形成过程:
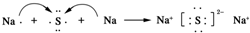 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.(4)表示①与⑦的化合物的电子式
 ,该化合物是由极性(填“极性”、“非极性”)键形成的.
,该化合物是由极性(填“极性”、“非极性”)键形成的.(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是S2->Cl->O2-.
(6)元素③的氢化物的结构式为H-O-H;该氢化物常温下和元素⑦的单质反应的化学方程式为Cl2+H2O═HClO+HCl.
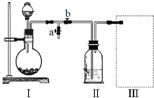
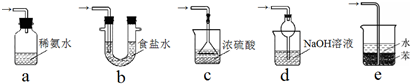
15.某校化学小组设计如图的装置制备氯气并探究氯气的某些化学性质:
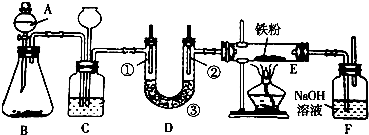
(1)欲利用浓盐酸与B不加热制取氯气,则B可选用下列物质中的bc;
a.MnO2 b.Ca(ClO)2 c.KMnO4 d.NaCl
(2)C装置的作用是安全瓶;C中加入饱和食盐水 溶液;当C后面的装置发生堵塞时,C中的现象是:长颈漏斗中液面上升.
(3)装置D用于验证氯气的漂白性,①是湿润的有色布条 ③是无水氯化钙或五氧化二磷
(4)为探究氯气与Fe反应的产物与氯气通入量的关系,设计实验,并记录现象如下:
根据实验结论,氯气与Fe粉共热时发生反应的化学方程式:2Fe+3Cl2=2FeCl3.

(1)欲利用浓盐酸与B不加热制取氯气,则B可选用下列物质中的bc;
a.MnO2 b.Ca(ClO)2 c.KMnO4 d.NaCl
(2)C装置的作用是安全瓶;C中加入饱和食盐水 溶液;当C后面的装置发生堵塞时,C中的现象是:长颈漏斗中液面上升.
(3)装置D用于验证氯气的漂白性,①是湿润的有色布条 ③是无水氯化钙或五氧化二磷
(4)为探究氯气与Fe反应的产物与氯气通入量的关系,设计实验,并记录现象如下:
| 实验方法 | 实验现象 | 实验结论 |
| 1.取反应初始阶段(氯气不足量)E中产物,用磁铁除去过量的Fe,剩余产物溶于水中,取上层溶液,①加入KSCN溶液,②加入KMnO4溶液 | ① ② | 生成物中没有FeCl2 生成物中含有FeCl3 |
| 2.取充分反应后(氯气通入足够长时间)E中产物,溶于水中,加入KMnO4溶液 | KSCN溶液显红色, KMnO4溶液不褪色 |
12.如图是某化学兴趣小组设计的利用电子垃圾(含70%Cu、25%Al、4%Fe及少量Au、Pt)制备硫酸铜和硫酸铝晶体的路线:
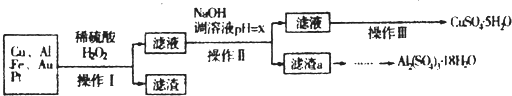
已知下列信息:Cu可与稀硫酸和H2O2的混合液反应生成硫酸铜;铁、铝、铜等离子以氢氧化物形式沉淀时溶液的pH如下表:
请回答下列问题:
(1)写出Cu与稀硫酸和H2O2的混合液反应的化学方程式(Cu+H2O2+H2SO4=CuSO4+2H2O..
(2)在操作II中,x的取值范围是[5.2,5.4).
(3)在操作III中,蒸发浓缩需要的玻璃仪器有玻璃棒、酒精灯、烧杯.
(4)由滤渣a制取Al2(SO4)3.18H2O,探究小组设计了三种方案:
甲:滤渣a$\stackrel{H_{2}SO_{4}}{→}$酸浸液$\stackrel{操作置}{→}$Al2(SO4)3.18H2O
乙:滤渣a$\stackrel{H_{2}SO_{4}}{→}$酸浸液$→_{过滤}^{适量Al粉}$过滤$\stackrel{操作置}{→}$Al2(SO4)3.18H2O
丙:滤渣a$→_{过滤}^{NaOH溶液}$滤液$\stackrel{H_{2}SO_{4}}{→}$溶液液$\stackrel{操作置}{→}$Al2(SO4)3.18H2O
综合考虑上述三种方案,最具可行性的是乙(填序号).
(5)为测定CuSO4.5H2O晶体的纯度,进行下列实验:取a g 试样配成100mL溶液,每次取20.00mL,消除干扰离子后,用b mol.L-1EDTA(Na2H2Y)标准溶液滴定其中的Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,平均消耗EDTA溶液12.00mL,CuSO4.5H2O晶体的纯度是$\frac{15b}{a}$×100%.
0 170651 170659 170665 170669 170675 170677 170681 170687 170689 170695 170701 170705 170707 170711 170717 170719 170725 170729 170731 170735 170737 170741 170743 170745 170746 170747 170749 170750 170751 170753 170755 170759 170761 170765 170767 170771 170777 170779 170785 170789 170791 170795 170801 170807 170809 170815 170819 170821 170827 170831 170837 170845 203614

已知下列信息:Cu可与稀硫酸和H2O2的混合液反应生成硫酸铜;铁、铝、铜等离子以氢氧化物形式沉淀时溶液的pH如下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 3.2 | 5.2 | 6.7 |
(1)写出Cu与稀硫酸和H2O2的混合液反应的化学方程式(Cu+H2O2+H2SO4=CuSO4+2H2O..
(2)在操作II中,x的取值范围是[5.2,5.4).
(3)在操作III中,蒸发浓缩需要的玻璃仪器有玻璃棒、酒精灯、烧杯.
(4)由滤渣a制取Al2(SO4)3.18H2O,探究小组设计了三种方案:
甲:滤渣a$\stackrel{H_{2}SO_{4}}{→}$酸浸液$\stackrel{操作置}{→}$Al2(SO4)3.18H2O
乙:滤渣a$\stackrel{H_{2}SO_{4}}{→}$酸浸液$→_{过滤}^{适量Al粉}$过滤$\stackrel{操作置}{→}$Al2(SO4)3.18H2O
丙:滤渣a$→_{过滤}^{NaOH溶液}$滤液$\stackrel{H_{2}SO_{4}}{→}$溶液液$\stackrel{操作置}{→}$Al2(SO4)3.18H2O
综合考虑上述三种方案,最具可行性的是乙(填序号).
(5)为测定CuSO4.5H2O晶体的纯度,进行下列实验:取a g 试样配成100mL溶液,每次取20.00mL,消除干扰离子后,用b mol.L-1EDTA(Na2H2Y)标准溶液滴定其中的Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,平均消耗EDTA溶液12.00mL,CuSO4.5H2O晶体的纯度是$\frac{15b}{a}$×100%.



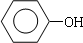 +(CH3)3CCl $\stackrel{无水AlCl_{3}}{→}$
+(CH3)3CCl $\stackrel{无水AlCl_{3}}{→}$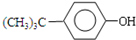 +HCl.
+HCl.