1.如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( )


| A. | X和R在同一周期 | |
| B. | 原子半径:W>R>X | |
| C. | 气态氢化物的稳定性:Y>X | |
| D. | X、Z可形成化学式为Z2X和Z2X2的化合物 |
20.N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g)?4NO2(g)+O2(g)-Q(Q>0)
一定温度时,向密闭容器中通入N2O5,部分实验数据见下表:
下列说法中错误的是( )
一定温度时,向密闭容器中通入N2O5,部分实验数据见下表:
| 时间/s | 0 | 500 | 1000 | 1500 |
| C(N2O5)/mol/L | 0.50 | 0.35 | 0.25 | 0.25 |
| A. | 500 s时O2的浓度为0.075 mol/L | |
| B. | 平衡后,升高温度,正反应速率先增大后减小 | |
| C. | 平衡后,要使平衡常数增大,改变的条件是升高温度 | |
| D. | 1000 s时将容器的体积缩小一半,重新达到平衡时0.25 mol/L<c(N2O5)<0.50 mol/L |
17.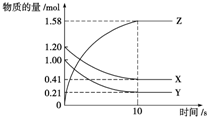 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应在0~10 s内,用Z表示的反应速率为0.158 mol•L-1•s-1 | |
| B. | 反应在0~10 s内,X的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应进行到10 s时,Y的转化率为79.0% | |
| D. | 反应的化学方程式为X(g)+Y(g)═Z(g) |
15.在体积为1L的两个恒容密闭容器中,分别充入1molCO和1molH2O(g)的混合气体,进行如下化学反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
(1)1100℃时,前10min该反应的化学反应速率v(CO2)=0.025mol/(L.min).
(2)计算1100℃时该反应的化学平衡常数K=$\frac{4}{9}$.
(3)能判断该反应是否达到化学平衡状态的依据是bc.
(a)容器中压强不变
(b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O)
(d)c(CO2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),平衡向右移动(选填“向右”或“向左”或“不”),再达到平衡时,H2百分含量不变(选填“增大”或“减小”或“不变”).
0 170620 170628 170634 170638 170644 170646 170650 170656 170658 170664 170670 170674 170676 170680 170686 170688 170694 170698 170700 170704 170706 170710 170712 170714 170715 170716 170718 170719 170720 170722 170724 170728 170730 170734 170736 170740 170746 170748 170754 170758 170760 170764 170770 170776 170778 170784 170788 170790 170796 170800 170806 170814 203614
| 0min | 10min | 20min | 30min | 40min | 50min | |
| 830℃ | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100℃ | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |
(2)计算1100℃时该反应的化学平衡常数K=$\frac{4}{9}$.
(3)能判断该反应是否达到化学平衡状态的依据是bc.
(a)容器中压强不变
(b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O)
(d)c(CO2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),平衡向右移动(选填“向右”或“向左”或“不”),再达到平衡时,H2百分含量不变(选填“增大”或“减小”或“不变”).
 .
.