19.下列有关主族元素M、N非金属性强弱比较的说明中,正确的是( )
| 事实 | 非金属 | |
| A | 第I电离能 M<N | M>N |
| B | 电负性M=N | M=N |
| C | 基态原子价层电子排布 M:nsnnpn+3,N:nsnnpn+4 | M>n |
| D | 原子半径 M>N | M<N |
| A. | A | B. | B | C. | C | D. | D |
17.某有机物甲经氧化后得乙(分子式为C2H302C1),而甲经水解可得丙.1mol丙和2mol乙反应得一种含氯的酯(C6H804Cl2),由此推断甲的结构简式为( )
| A. | HCOOCH2Cl | B. | ClCH2CH2OH | C. | CH2ClCHO | D. | HOCH2CH2OH |
15. 某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
I.该同学推测,铝热反应所得到的熔融物应是铁铝合金.理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金.请你设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是NaOH溶液,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
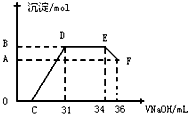
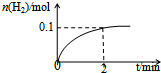
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子为:H++OH-═H2O.
(2)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方为NH4++OH-═NH3•H2O.
(3)当c=13mL时,原溶液中Fe3+与Al3+的物质的量之比为2:1.
0 170112 170120 170126 170130 170136 170138 170142 170148 170150 170156 170162 170166 170168 170172 170178 170180 170186 170190 170192 170196 170198 170202 170204 170206 170207 170208 170210 170211 170212 170214 170216 170220 170222 170226 170228 170232 170238 170240 170246 170250 170252 170256 170262 170268 170270 170276 170280 170282 170288 170292 170298 170306 203614
 某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | -- |
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子为:H++OH-═H2O.
(2)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方为NH4++OH-═NH3•H2O.
(3)当c=13mL时,原溶液中Fe3+与Al3+的物质的量之比为2:1.

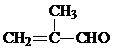 ;J的结构简式为
;J的结构简式为 .
. +
+ $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O.
+H2O.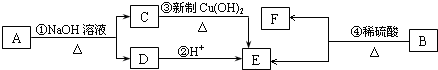
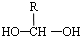 $\stackrel{-H_{2}O}{→}$
$\stackrel{-H_{2}O}{→}$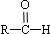 (R代表烃基).
(R代表烃基).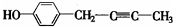 、
、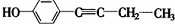 .
. .
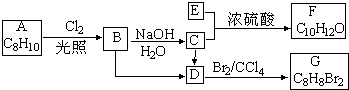
.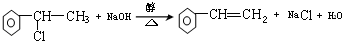 ,E+C→F
,E+C→F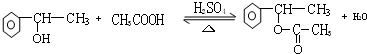
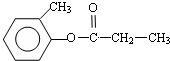
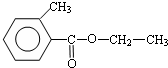
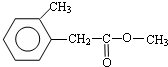

 .
.
 化学平衡:
化学平衡:

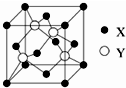 元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.