9.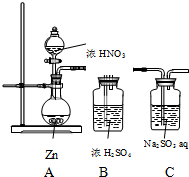 甲同学探究NO2的氧化性;设计了如下实验装置:
甲同学探究NO2的氧化性;设计了如下实验装置:
(1)该装置的明显缺陷是:无尾气处理装置
(2)实验开始后,发现Zn溶解,但未发现有气体逸出,同学猜想可能是因为HNO3被还原生成NH4+写出反应的离子方程式:4Zn+NO3-+10H+=4Zn2++NH4++3H2O 如何验证该猜想:取少量A中反应后的溶液置于试管中,向其中滴加少量氢氧化钠溶液,并加热,在试管口处放置一张湿润的红色石蕊试纸,若试纸变蓝,则猜想成立
(3)重新调整HNO3浓度后,发现A中有红棕色气体逸出,设计实验,证明NO2具有氧化性(药品意选择,合理即可)
(4)乙同学对甲的实验结果产生质疑,提出假设:
假一:NO2氧化了SO32-
假设二:HNO3氧化了SO32-
问题1:假设二是(“是”或“否”)合理,
理由:3NO2+H2O=2HNO3+NO(用化学方程式回答)
问题2:若要验证NO2具有氧化性,你的实验方案是:在一个真空密闭容器中同时通入NO2和SO2,一段时间后,容器中气体的红棕色褪去,证明了二者发生了反应,证明了NO2的氧化性.
 甲同学探究NO2的氧化性;设计了如下实验装置:
甲同学探究NO2的氧化性;设计了如下实验装置:(1)该装置的明显缺陷是:无尾气处理装置
(2)实验开始后,发现Zn溶解,但未发现有气体逸出,同学猜想可能是因为HNO3被还原生成NH4+写出反应的离子方程式:4Zn+NO3-+10H+=4Zn2++NH4++3H2O 如何验证该猜想:取少量A中反应后的溶液置于试管中,向其中滴加少量氢氧化钠溶液,并加热,在试管口处放置一张湿润的红色石蕊试纸,若试纸变蓝,则猜想成立
(3)重新调整HNO3浓度后,发现A中有红棕色气体逸出,设计实验,证明NO2具有氧化性(药品意选择,合理即可)
| 步骤 | 现象 | 结论 |
| 取少量C中反应后的溶液 置于试管中, 先加入盐酸溶液酸化,再加入 氯化钡溶液 | 有白色沉淀产生 | NO2具有氧化性 |
假一:NO2氧化了SO32-
假设二:HNO3氧化了SO32-
问题1:假设二是(“是”或“否”)合理,
理由:3NO2+H2O=2HNO3+NO(用化学方程式回答)
问题2:若要验证NO2具有氧化性,你的实验方案是:在一个真空密闭容器中同时通入NO2和SO2,一段时间后,容器中气体的红棕色褪去,证明了二者发生了反应,证明了NO2的氧化性.
8.一定条件下将0.5mol SO2和一定量O2通入恒容密闭容器中,压强为4.04×105Pa,在恒温(500℃)下反应达到平衡,压强为3.03×105Pa,测得余0.1mol O2,则SO2的转化率为( )
| A. | 80% | B. | 75% | C. | 60% | D. | 40% |
7.下列反应的离子方程式正确的是( )
| A. | 向碳酸氢铵溶液中加入过量的氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| B. | 钠投入水中:Na+H2O═Na++OH-+H2↑ | |
| C. | 将少量二氧化碳通入水玻璃中:CO2+SiO32-+H2O═CO32-+H2SiO3↓ | |
| D. | 氯气通入水中:Cl2+H2O═2H++Cl-+ClO- |
6.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 1 mol H2O含有的原子数为NA | |
| B. | 4g H2含有氢分子数4NA | |
| C. | 1L 0.1 mol•L-1NaCl溶液中含Na+数0.1NA | |
| D. | 常温常压下,11.2L O2中含有分子数为0.5NA |
4.某元素原子核内质子数为m,中子数为n,则下列论断正确的是( )
| A. | 这种元素的相对原子质量为m+n | |
| B. | 若碳原子质量为wg,则此原子的质量为(m+n)wg | |
| C. | 不能由此确定该元素的相对原子质量 | |
| D. | 核内中子的总质量小于质子的总质量 |
3.已知下列键能数据,则反应:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g)△H为( )
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ•mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
| A. | 236 kJ•mol-1 | B. | -116 kJ•mol-1 | C. | -236 kJ•mol-1 | D. | 116 kJ•mol-1 |
2.下列关于各实验装置图的叙述中,正确的是( )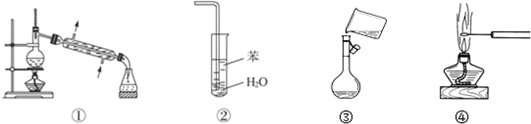

| A. | 装置①常用于分离互不相溶的液体混合物 | |
| B. | 装置②可用于吸收NH3,并防止倒吸 | |
| C. | 图③是将溶解好的溶液转移到容量瓶中 | |
| D. | 图④可观察NaCl的焰色反应 |
1.实验室下列物质的保存方法中,不正确的是( )
| A. | 氢氧化钠溶液盛装在用橡胶塞的试剂瓶中 | |
| B. | 氢氟酸盛装在细口玻璃瓶中 | |
| C. | 硫酸亚铁溶液存放在加有少量铁粉的试剂瓶中 | |
| D. | 金属钠保存在石蜡油或煤油中 |
20.已知 2SO2(g)+O2(g)?2SO3△H=-197KJ/mol下列说法正确的是( )
0 169451 169459 169465 169469 169475 169477 169481 169487 169489 169495 169501 169505 169507 169511 169517 169519 169525 169529 169531 169535 169537 169541 169543 169545 169546 169547 169549 169550 169551 169553 169555 169559 169561 169565 169567 169571 169577 169579 169585 169589 169591 169595 169601 169607 169609 169615 169619 169621 169627 169631 169637 169645 203614
| A. | 其他条件不变,改变反应物的量,△H发生改变 | |
| B. | 上述反应生成1mol SO3,放热少于98.5KJ | |
| C. | 相同条件下加入2molSO2(g)、1mol O2(g) 充分反应放热等于197KJ | |
| D. | 相同条件下加入1molSO2(g)、0.5mol O2(g) 充分反应放热为Q1 kJ,若在相同容器中加入1mol SO3充分反应吸热等于Q2kJ,Q1kJ+Q2 kJ=98.5kJ |