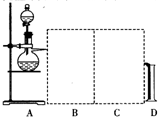
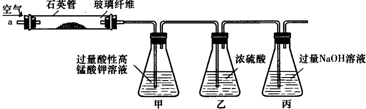
8.某元素原子的最外层上只有2个电子,该元素是( )
| A. | 一定是IIA元素 | |
| B. | 一定是金属元素 | |
| C. | 一定是正二价元素 | |
| D. | 可能是金属元素,也可能是非金属元素 |
4.化合物丙由如下反应得到:
C4H10O $\stackrel{H_{2}SO_{4}(浓),△}{→}$C4H8$→_{溶剂CCl_{4}}^{Br_{2}}$C4H8Br2(丙),丙的结构简式不可能是( )
C4H10O $\stackrel{H_{2}SO_{4}(浓),△}{→}$C4H8$→_{溶剂CCl_{4}}^{Br_{2}}$C4H8Br2(丙),丙的结构简式不可能是( )
| A. | CH3CH2CHBrCH2Br | B. | CH3CH(CH2Br)2 | C. | CH3CHBrCHBrCH3 | D. | (CH3)2CBrCH2Br |
3.下列物质既能发生消去反应生成相应的烯烃,又能氧化生成相应醛的是( )
| A. | CH3OH | B. | CH3CH2CH2OH | C. | 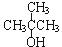 | D. | 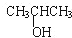 |
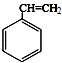
2.桶烯结构简式如图所示,有关说法不正确的是( )
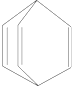

| A. | 桶烯在一定条件下能发生加聚反应 | |
| B. | 桶烯与苯乙烯(C6H5CH═CH2)互为同分异构体 | |
| C. | 桶烯中的一个氢原子被氯原子取代,所得产物只有两种 | |
| D. | 桶烯分子中所有的原子在同一平面上 |
1.苯酚环上含有-C4H9基团的同分异构体有( )
0 167487 167495 167501 167505 167511 167513 167517 167523 167525 167531 167537 167541 167543 167547 167553 167555 167561 167565 167567 167571 167573 167577 167579 167581 167582 167583 167585 167586 167587 167589 167591 167595 167597 167601 167603 167607 167613 167615 167621 167625 167627 167631 167637 167643 167645 167651 167655 167657 167663 167667 167673 167681 203614
| A. | 3种 | B. | 9种 | C. | 12种 | D. | 6种 |
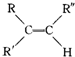 $→_{H_{2}SO_{4}}^{KMnO_{4}}$
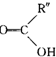
$→_{H_{2}SO_{4}}^{KMnO_{4}}$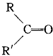 +
+
 例如:
例如: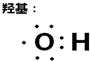
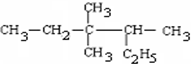 的名称3,3,4-三甲基己烷
的名称3,3,4-三甲基己烷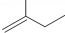 的名称2-甲基-1-丁烯.
的名称2-甲基-1-丁烯.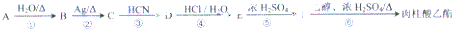
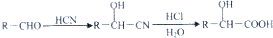
 ,肉酸乙酯的结构简式
,肉酸乙酯的结构简式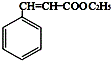 .
.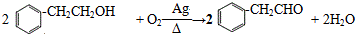 .
.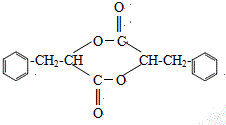 ;H是另一种副产物,它 是一种高分子化合物,形成这种物质的反应类型为缩聚反应.
;H是另一种副产物,它 是一种高分子化合物,形成这种物质的反应类型为缩聚反应.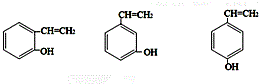 (填结构简式).
(填结构简式).