题目内容
1.苯酚环上含有-C4H9基团的同分异构体有( )| A. | 3种 | B. | 9种 | C. | 12种 | D. | 6种 |
分析 -C4H9有四种结构,分别为:CH3-CH2-CH2-CH2-、CH3-CH2-CH(CH3)-、(CH3)2CH-CH2-、(CH3)3C-,苯环上的两个取代基位置可以有邻、间、对三种,据此解答即可.
解答 解:-C4H9有四种结构,分别为:CH3-CH2-CH2-CH2-、CH3-CH2-CH(CH3)-、(CH3)2CH-CH2-、(CH3)3C-,苯酚上含有1个羟基,此时分为邻间对三种取代位置,故总共有同分异构体数目为4×3=12种,故选C.
点评 本题主要考查的是同分异构体的判断,掌握丁基有四种结构以及苯环上的二元取代有邻、间、对三种情况,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.2005年10月5日瑞典皇家科学院在瑞典首都斯德哥尔摩宣布,法国人伊夫•肖万、美国人罗伯特•格拉布和理查德•施罗克,因在烯烃复分解反应研究方面的贡献而荣获2005年度诺贝尔化学奖.在石油化工中,利用烯烃复分解反应可以将丁烯和乙烯转化为丙烯,方程式如下:CH3CH=CHCH3+CH2=CH2$\stackrel{催化剂}{→}$2CH2=CHCH3从反应类型上看,该反应还可看作( )
| A. | 取代反应 | B. | 加成反应 | C. | 消去反应 | D. | 裂解反应 |
12.向NaBr和NaI混合溶液中通入足量氯气后,将溶液蒸干并灼烧,最后得到的物质是( )
| A. | NaBr和NaI | B. | NaCl | C. | NaBr和NaCl | D. | NaCl和 I2 |
13.中小学生使用的涂改液被称为“隐形杀手”,是因为涂改液里主要含有二甲苯 等有机烃类物质,长期接触二甲苯会对血液循环系统产生损害,可导致再生障碍性贫血和骨髓综合症(白血病的前期).下列说法不正确的是( )
| A. | 二甲苯有三种同分异构体 | |
| B. | 二甲苯和甲苯是同系物 | |
| C. | 二甲苯分子中,所有碳原子都在同一个平面上 | |
| D. | 1mol二甲苯完全燃烧后,生成的二氧化碳和水的物质的量相等 |
10.化学与生活密切相关,下列说法正确的是( )
| A. | 聚乙烯塑料的老化是由于发生了加成反应 | |
| B. | 地沟油的主要成分是油脂,其组成与汽油、煤油相同 | |
| C. | 合成纤维、人造纤维及光导纤维都属于有机高分子材料 | |
| D. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
11.某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):关于该固体混合物,下列说法正确的是( )


| A. | 一定含有Al,其质量为4.5g | |
| B. | 一定不含FeCl2,可能含有MgCl2和AlCl3 | |
| C. | 一定含有MgCl2和FeCl2 | |
| D. | 一定含有(NH4)2SO4和MgCl2,且物质的量相等 |

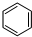 -CH3(g)+11H2△H=kJ•mol-1.
-CH3(g)+11H2△H=kJ•mol-1.