13.下列有关说法错误的是( )
| A. | 催化剂通过降低化学反应的焓变加快化学反应速率 | |
| B. | 反应N2(g)+3H2(g)═2NH3(g)(△H<0)达平衡后,降低温度,正反应速率增大、逆反应速率减小,平衡向正反应方向移动 | |
| C. | 反应NH3(g)+HCl(g)═NH4Cl(s)低温下能自发进行,说明该反应的△H<0 | |
| D. | 用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗盐酸的体积更大 |
12.关于如图各实验装置的叙述中,不正确的是( )

| A. | 利用图1装置可用于实验室制取少量NH3或O2 | |
| B. | 用图2可证明Cl2的氧化性强于S | |
| C. | 用图3所示装置可分离CH3CH2OH和CH3COOC2H5混合液 | |
| D. | 用图4所示装置可制取乙烯并验证其易被氧化 |
11.X、Y、Z、W为四种短周期元素,它们在周期表中位于连续的四个主族,如表所示.Z元素原子最外层电子数是内层电子总数的$\frac{1}{5}$.下列说法正确的是( )
| X | Y | ||
| Z | W |
| A. | 原子半径由小到大的顺序为X<Y<Z<W | |
| B. | Y元素最高价氧化物对应的水化物化学式为H3YO4 | |
| C. | X、Z两种元素的氧化物中所含化学键类型相同 | |
| D. | Y最简单气态氢化物比Y相邻周期同主族元素气态氢化物更加稳定 |
10.下列表示对应化学反应的离子方程式,其中正确的是( )
| A. | 苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| B. | NaHSO4溶液中加入Ba(OH)2溶液至SO42完全沉淀:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | (NH4)2Fe(SO4)2溶液中加入过量的氢氧化钡溶液:2NH4++Fe2++4OH-═Fe(OH)2↓+2NH3•H2O | |
| D. | 用惰性电极电解饱和氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- |
9.下列有关物质的性质和该性质的应用均正确的是( )
| A. | NH3溶于水后显碱性,在FeCl3饱和溶液中通入足量NH3可制取Fe(OH)3胶体 | |
| B. | 油脂在碱性条件下易水解,可用于制作肥皂 | |
| C. | 次氯酸钠具有强还原性,可用于配制“84”消毒液 | |
| D. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
8.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液:Na+、NH4+、S2-、NO3- | |
| B. | c(HSO4-)=0.1 mol/L的溶液:K+、Ba2+、HCO3-、Cl- | |
| C. | 滴入少量苯酚显紫色的溶液:Na+、K+、I-、SO42- | |
| D. | 能溶解碳酸钙的溶液:Na+、NH4+、Cl-、Br- |
7.已知阿伏加德罗常数的值为NA,下列说法正确的是( )
| A. | 1 mol CH3+(甲基碳正离子)含有的电子数目为9NA | |
| B. | 7.2g C5H12含有的C-C键的数目为0.5NA | |
| C. | 常温常压条件下,14 g N2和CO的混合气体含有的分子数目为0.5NA | |
| D. | 2mol H2O2完全分解生成1mol O2,转移的电子数为4NA |
6.下列有关化学用语表示正确的是( )
0 167374 167382 167388 167392 167398 167400 167404 167410 167412 167418 167424 167428 167430 167434 167440 167442 167448 167452 167454 167458 167460 167464 167466 167468 167469 167470 167472 167473 167474 167476 167478 167482 167484 167488 167490 167494 167500 167502 167508 167512 167514 167518 167524 167530 167532 167538 167542 167544 167550 167554 167560 167568 203614
| A. | 中子数为21的钾原子:${\;}_{19}^{40}$K | |
| B. | 氯化钡的电子式:Ba2+[${\;}_{•}^{•}$$\underset{\stackrel{••}{ci}}{••}$${\;}_{•}^{•}$]${\;}_{2}^{-}$ | |
| C. | N3-的结构示意图: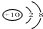 | |
| D. | 聚2-甲基-1,3-丁二烯的结构简式: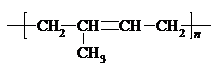 |