7.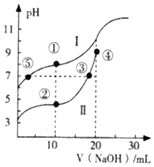 常温下,用0.10mol•L-1NaOH溶液分别滴定20.00mL浓度均为 0.10mol•L-1的CH3COOH(Ka=1.75×10-5)溶液和HCN (Ka=4.9×10-10)溶液所得滴定曲线如图.下列说法正确的是( )
常温下,用0.10mol•L-1NaOH溶液分别滴定20.00mL浓度均为 0.10mol•L-1的CH3COOH(Ka=1.75×10-5)溶液和HCN (Ka=4.9×10-10)溶液所得滴定曲线如图.下列说法正确的是( )
 常温下,用0.10mol•L-1NaOH溶液分别滴定20.00mL浓度均为 0.10mol•L-1的CH3COOH(Ka=1.75×10-5)溶液和HCN (Ka=4.9×10-10)溶液所得滴定曲线如图.下列说法正确的是( )
常温下,用0.10mol•L-1NaOH溶液分别滴定20.00mL浓度均为 0.10mol•L-1的CH3COOH(Ka=1.75×10-5)溶液和HCN (Ka=4.9×10-10)溶液所得滴定曲线如图.下列说法正确的是( )| A. | 曲线I和曲线Ⅱ分别代表的是CH3COOH和HCN | |
| B. | 点③和点⑤所示溶液中:c(CN-)=c(CH3COO-) | |
| C. | 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH) | |
| D. | 在点②和③之间(不包括端点)存在关系:c(Na+)>c(A-)>c(H+)>c(OH-) (A-代表溶液中的酸根离子) |
6. 用AG表示溶液酸度:AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.在室温下,用0.1mol/L的HCl溶液滴定20.00mL0.1mol/L氨水.滴定结果可表示如图:下列分析正确的是( )
用AG表示溶液酸度:AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.在室温下,用0.1mol/L的HCl溶液滴定20.00mL0.1mol/L氨水.滴定结果可表示如图:下列分析正确的是( )
 用AG表示溶液酸度:AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.在室温下,用0.1mol/L的HCl溶液滴定20.00mL0.1mol/L氨水.滴定结果可表示如图:下列分析正确的是( )
用AG表示溶液酸度:AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.在室温下,用0.1mol/L的HCl溶液滴定20.00mL0.1mol/L氨水.滴定结果可表示如图:下列分析正确的是( )| A. | 0.lmol/L 氨水 pH=10.2 | |
| B. | A点加入盐酸的体积为20.00mL | |
| C. | 若a=7,从A到B水的电离程度逐渐减小 | |
| D. | B点溶液中可能存在c(Cl-)>c(NH4+)>(H+)>c(OH-) |
3. 常温下,体积均为50.00mL、浓度均为0.1000mol/L的NaCl、NaBr及NaI三种溶液,分别用0.1000mol/L的AgNO3溶液滴定,滴定曲线如图所示:
常温下,体积均为50.00mL、浓度均为0.1000mol/L的NaCl、NaBr及NaI三种溶液,分别用0.1000mol/L的AgNO3溶液滴定,滴定曲线如图所示:
已知:p Ag+=-lgc(Ag+),Ksp(AgI)=8.0×10-17,Ksp(AgBrI)=5.0×10-13,Ksp(AgCl)=1.8×10-10.下列说法正确的是( )
 常温下,体积均为50.00mL、浓度均为0.1000mol/L的NaCl、NaBr及NaI三种溶液,分别用0.1000mol/L的AgNO3溶液滴定,滴定曲线如图所示:
常温下,体积均为50.00mL、浓度均为0.1000mol/L的NaCl、NaBr及NaI三种溶液,分别用0.1000mol/L的AgNO3溶液滴定,滴定曲线如图所示:已知:p Ag+=-lgc(Ag+),Ksp(AgI)=8.0×10-17,Ksp(AgBrI)=5.0×10-13,Ksp(AgCl)=1.8×10-10.下列说法正确的是( )
| A. | 三种溶液各取10 mL混合,然后滴定,沉淀先后顺序为Cl-、Br-、I- | |
| B. | 滴定Cl-时,可加人少量的KI作指示剂 | |
| C. | 当滴定AgNO3溶液至70.00mL时,溶液中c(I-)>c (Br-)>c(Cl-) | |
| D. | 滴定曲线①、②、③分别表示NaI溶液、NaBr溶液、NaCl溶液 |
2. 常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子浓度变化如图所示,下列有关说法正确的是( )
常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子浓度变化如图所示,下列有关说法正确的是( )
 常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子浓度变化如图所示,下列有关说法正确的是( )
常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子浓度变化如图所示,下列有关说法正确的是( )| A. | 常温下,PbI2的Ksp为2×10-6 | |
| B. | 温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,PbI2的溶解度不变,Pb2+浓度不变 | |
| C. | T时刻改变的条件是升高温度,因而PbI2的Ksp增大 | |
| D. | 常温下Ksp(PbS)=8×10 -28,向PbI2的悬浊液中加入Na2S溶液,PbI2 (s)+S2- (aq) PbS(s)+2I- (aq)反应的化学平衡常数为5×l018 |
1.下列说法不正确的是( )
| A. | σ键比π键重叠程度大,形成的共价键强 | |
| B. | 两个原子之间形成共价键时,最多有一个σ键 | |
| C. | 气体单质中,一定有σ键,可能有π键 | |
| D. | N2分子中有一个σ键,2个π键 |
2.下列离子组一定能大量共存的是( )
| A. | pH=12的溶液:K+、Na+、CH3COO-、Br- | |
| B. | 由水电离出c(H+)=10-3mol/L的溶液中:Na+、[Al(OH)4]-、NO3-、HCO3- | |
| C. | 无色溶液中可能大量共存在Fe3+、NH4+、Cl-、S2- | |
| D. | 1mol/L的KNO3溶液:H+、Fe2+、Cl-、SO42- |
1.用氢氧化钠固体配制480mL 0.1mol/LNaOH溶液时,下列有关说法正确的是( )
| A. | 用到的玻璃仪器只有有:玻璃棒、烧杯 | |
| B. | 洗净的容量瓶必须干燥后才能用 | |
| C. | 称量2.0g氢氧化钠固体 | |
| D. | 没有等溶液冷却就转移,或定容时俯视,均导致所配溶液浓度偏低 |
20.能正确表示下列反应的离子方程式为( )
0 163702 163710 163716 163720 163726 163728 163732 163738 163740 163746 163752 163756 163758 163762 163768 163770 163776 163780 163782 163786 163788 163792 163794 163796 163797 163798 163800 163801 163802 163804 163806 163810 163812 163816 163818 163822 163828 163830 163836 163840 163842 163846 163852 163858 163860 163866 163870 163872 163878 163882 163888 163896 203614
| A. | NaClO和NaOH的混合溶液中通入少量的SO2:ClO-+H2O+SO2=C1-+SO42-+2H+ | |
| B. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O | |
| C. | 硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ | |
| D. | 大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |

 洁净煤技术(CCT)是煤的高效清洁利用的技术.煤中的硫主要以黄铁矿(FeS2)为主,其次为磁硫铁矿(Fe7S8)、闪锌矿(ZnS)、方铅矿(PbS)等.回答下列问题:
洁净煤技术(CCT)是煤的高效清洁利用的技术.煤中的硫主要以黄铁矿(FeS2)为主,其次为磁硫铁矿(Fe7S8)、闪锌矿(ZnS)、方铅矿(PbS)等.回答下列问题: .
.