2.(1)工业合成氨时,合成塔中每产生1molNH3,放出46.1kJ的热量.
某小组研究在500℃下该反应过程中的能量变化.他们分别在体积均为VL的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应.相关数据如表:
①容器a中,0~t1时间的平均反应速率为υ(H2)=$\frac{1.2}{{V{t_1}}}$mol•L-1•min-1.
②下列叙述正确的是AD(填字母序号).
A.容器b中反应达平衡状态时,Q>73.76kJ
B.平衡时,两容器中H2的体积分数相等
C.反应开始时,两容器中反应的化学反应速率相等
D.平衡时,容器中N2的转化率:a<b
(2)以氨为原料,合成尿素的反应原理为:
2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g)△H=a kJ•mol-1.
为研究平衡时CO2的转化率与反应物投料比[$\frac{n(CO₂)}{n(NH₃)}$]及温度的关系,研究小组在10 L恒容密闭容器中进行模拟反应.(如图1,Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系).

①a<0 (填“>”或“<”).
②若n(CO2)起始=10 mol,曲线Ⅱ的投料比为0.4,在100℃条件下发生反应,达平衡至A点,则A点与起始压强比为5:7.
③A点平衡常数与B点平衡常数间的关系:KA= KB (填“>”或“<”或“=”).
(3)利用氨气与空气催化氧化法制取联氨N2H4.如图2是由“联氨-空气”形成的绿色燃料电池,以石墨为电极的电池工作原理示意图,b电极为正极(填“正”或“负”),写出该电池工作时a电极的电极反应式N2H4-4e-=N2+4H+.
某小组研究在500℃下该反应过程中的能量变化.他们分别在体积均为VL的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应.相关数据如表:
| 容器 | 起始时各物质物质的量/mol | 达到平衡的时间 | 达平衡时体系能量的变化/kJ | ||
| N2 | H2 | NH3 | |||
| a | 1 | 4 | 0 | t1 min | 放出热量:36.88kJ |
| b | 2 | 8 | 0 | t2 min | 放出热量:Q |
②下列叙述正确的是AD(填字母序号).
A.容器b中反应达平衡状态时,Q>73.76kJ
B.平衡时,两容器中H2的体积分数相等
C.反应开始时,两容器中反应的化学反应速率相等
D.平衡时,容器中N2的转化率:a<b
(2)以氨为原料,合成尿素的反应原理为:
2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g)△H=a kJ•mol-1.
为研究平衡时CO2的转化率与反应物投料比[$\frac{n(CO₂)}{n(NH₃)}$]及温度的关系,研究小组在10 L恒容密闭容器中进行模拟反应.(如图1,Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系).

①a<0 (填“>”或“<”).
②若n(CO2)起始=10 mol,曲线Ⅱ的投料比为0.4,在100℃条件下发生反应,达平衡至A点,则A点与起始压强比为5:7.
③A点平衡常数与B点平衡常数间的关系:KA= KB (填“>”或“<”或“=”).
(3)利用氨气与空气催化氧化法制取联氨N2H4.如图2是由“联氨-空气”形成的绿色燃料电池,以石墨为电极的电池工作原理示意图,b电极为正极(填“正”或“负”),写出该电池工作时a电极的电极反应式N2H4-4e-=N2+4H+.
14.如果以乙烯为原料,经过两步反应制得乙二醇,则这两步反应的类型依次是( )
| A. | 加成反应、取代反应 | B. | 加成反应、消去反应 | ||
| C. | 取代反应、消去反应 | D. | 取代反应、加成反应 |
13.已知25℃时有关弱酸的电离平衡常数:
现维持25℃,下列有关说法正确的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7K2=5.6×l0-11 |
| A. | 等物质的量浓度的各溶液pH关系:pH(Na2CO3)>pH(CH3COONa)>pH(NaCN) | |
| B. | NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)c+(CO32-)+c(OH-) | |
| C. | 向PH=1的醋酸溶液中加水稀释,醋酸的电离度、pH均先增大后减小 | |
| D. | a mol•L-1HCN溶液与b mol•L-1NaOH溶液等体积混合,若pH=7,则a>b |
12.将等体积、等pH的NaOH溶液和NH3•H2O溶液,分别加入到盛有10mL1mol/LAlCl3溶液的甲、乙两烧杯中.下列说法正确的是( )
| A. | 甲中沉淀一定比乙多 | B. | 甲和乙中沉淀可能一样多 | ||
| C. | 甲中沉淀可能比乙多 | D. | 乙中沉淀一定比甲多 |
11. 化学在环境保护中起着十分重要的作用,电化学降解NO3-的原理如图所示.下列说法不正确的是 (相对原子质量 O-16)( )
化学在环境保护中起着十分重要的作用,电化学降解NO3-的原理如图所示.下列说法不正确的是 (相对原子质量 O-16)( )
 化学在环境保护中起着十分重要的作用,电化学降解NO3-的原理如图所示.下列说法不正确的是 (相对原子质量 O-16)( )
化学在环境保护中起着十分重要的作用,电化学降解NO3-的原理如图所示.下列说法不正确的是 (相对原子质量 O-16)( )| A. | A为电源的正极 | |
| B. | 溶液中H+从阳极向阴极迁移 | |
| C. | Ag-Pt电极的电极反应式为2NO3-+12H++10e-═N2↑+6H2O | |
| D. | 电解过程中,每转移2 mol电子,则左侧电极就产生32gO2 |
10.某有机物的结构简式如图所示  ,下列有关该有机物说法正确的是( )
,下列有关该有机物说法正确的是( )
0 163651 163659 163665 163669 163675 163677 163681 163687 163689 163695 163701 163705 163707 163711 163717 163719 163725 163729 163731 163735 163737 163741 163743 163745 163746 163747 163749 163750 163751 163753 163755 163759 163761 163765 163767 163771 163777 163779 163785 163789 163791 163795 163801 163807 163809 163815 163819 163821 163827 163831 163837 163845 203614
 ,下列有关该有机物说法正确的是( )
,下列有关该有机物说法正确的是( )| A. | 该有机物的化学式为C10H14 | |
| B. | 它的一氯代物有6种 | |
| C. | 它的分子中所有的碳原子一定在同一平面上 | |
| D. | 一定条件下,它可以发生取代、加成、氧化和还原反应 |

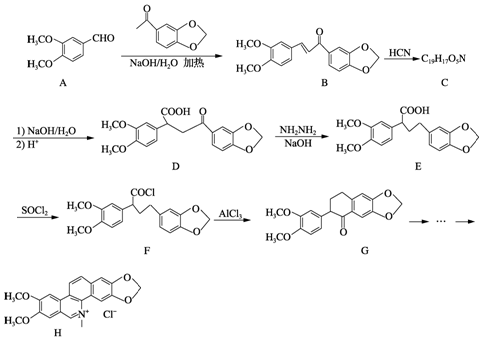
 ;由E→F的反应类型为取代.
;由E→F的反应类型为取代. .
. ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).

 .
. .
. .
.
 )
)
 .由甲苯生成甲的反应类型是取代反应.
.由甲苯生成甲的反应类型是取代反应. +HOCH2CH2Cl$→_{△}^{浓硫酸}$
+HOCH2CH2Cl$→_{△}^{浓硫酸}$ +H2O
+H2O .
.