19.将一定质量的乙炔(化学式为C2H2)和氧气放在密闭的容器中点燃,测得反应前后各物质的质量如下表:
该反应的化学方程式为4C2H2+9O2$\stackrel{点燃}{→}$4H2O+6CO2+2CO;若要使燃烧后无M生成,则需要氧气的质量为1.6g.
| 物质 | 乙炔 | 氧气 | 水 | 二氧化碳 | M |
| 反应前质量/g | 5.2 | 14.4 | 0.4 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 4.0 | m | 2.8 |
18.某有机物结构为 ,以下关于它的叙述正确的是( )
,以下关于它的叙述正确的是( )
 ,以下关于它的叙述正确的是( )
,以下关于它的叙述正确的是( )| A. | 其一氯代物有2种 | B. | 其二氯代物有5种 | ||
| C. | 其分子式为C10H14 | D. | 它常温下为气态 |
17.用下列实验装置进行相应实验,能达到实验目的是( )
| A. |  用图所示装置除去Cl2中含有的HCl | |
| B. | 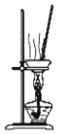 用图所示装置蒸干MgCl2饱和溶液制备MgCl2•6H2O晶体 | |
| C. |  用环己烷萃取碘水时将两者混合后需如图3所示用力振荡 | |
| D. |  继续煮沸图所示溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
15.短周期元素X、Y、Z、W、Q的原子序数依次增大,且只有一种金属元素,其中X与W处于同一主族,Z元素原子半径在短周期中最大(稀有气体除外),Z与W、W与Q的原子序数之差均为3,五种元素原子的最外层电子数之和为21,下列说法不正确的是( )
| A. | Q的单质能与Z的最高价氧化物的水化物发生氧化还原反应 | |
| B. | 气态氢化物的稳定性:Q>W | |
| C. | 一定条件下,Q的单质可把Y的单质从其氢化物中置换出来 | |
| D. | 最高价氧化物对应水化物的酸性顺序:Q>Y>W>X |
14.下列实验操作能达到实验目的是( )
| A. | 向苯酚浊液中滴加少量饱和Na2CO3溶液,浊液变澄清,证明结合质子的能力:CO32->C6H5O- | |
| B. | 配制Fe(NO3)2溶液时加入适量的硝酸,可抑制Fe2+水解 | |
| C. | 测定相同温度下相同浓度的碳酸钠和亚硫酸钠溶液的pH,前者大于后者,证明元素的非金属性:C<S | |
| D. | 用激光笔照射蛋白质溶液、硅酸溶胶,可将二者区分开 |
13. 在T℃时,将一定量A加入到体积为2L的某密闭容器中,发生以下化学反应:2A(g)?B(g)+C(g)△H=-akJ/mol.反应在第15min时达到平衡,反应过程中B、A的浓度比与时间t有如图所示关系,若测得第15min时c(B)=0.8mol/L,下列结论正确的是( )
在T℃时,将一定量A加入到体积为2L的某密闭容器中,发生以下化学反应:2A(g)?B(g)+C(g)△H=-akJ/mol.反应在第15min时达到平衡,反应过程中B、A的浓度比与时间t有如图所示关系,若测得第15min时c(B)=0.8mol/L,下列结论正确的是( )
 在T℃时,将一定量A加入到体积为2L的某密闭容器中,发生以下化学反应:2A(g)?B(g)+C(g)△H=-akJ/mol.反应在第15min时达到平衡,反应过程中B、A的浓度比与时间t有如图所示关系,若测得第15min时c(B)=0.8mol/L,下列结论正确的是( )
在T℃时,将一定量A加入到体积为2L的某密闭容器中,发生以下化学反应:2A(g)?B(g)+C(g)△H=-akJ/mol.反应在第15min时达到平衡,反应过程中B、A的浓度比与时间t有如图所示关系,若测得第15min时c(B)=0.8mol/L,下列结论正确的是( )| A. | 反应达平衡时,A的转化率为80% | |
| B. | A的初始物质的量为2mol | |
| C. | 反应到达平衡时,放出的热量是2a KJ | |
| D. | 15min时,v正=v逆=0 |
12.化学是一门实用性很强的科学,与社会、环境等密切相关.下列说法错误的是( )
| A. | 用CO2合成可降解的聚碳酸酯塑料,能减少白色污染及其危害 | |
| B. | 用含橙色酸性重铬酸钾的仪器检验酒驾,利用了乙醇的挥发性和还原性 | |
| C. | 浸泡过高锰酸钾溶液的硅藻土放于新鲜的水果箱内是为了催熟水果 | |
| D. | “煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气 |
11.在反应容器中充入1molA气体和n molB气体,在一定条件下发生反应:A(气)+nB(气)?mC(气),达平衡时,测得A的转化率为50%,在相同温度和相同压强下,平衡时混合气体的体积是反应前的$\frac{3}{4}$,则n和m的数值可能是( )
0 163166 163174 163180 163184 163190 163192 163196 163202 163204 163210 163216 163220 163222 163226 163232 163234 163240 163244 163246 163250 163252 163256 163258 163260 163261 163262 163264 163265 163266 163268 163270 163274 163276 163280 163282 163286 163292 163294 163300 163304 163306 163310 163316 163322 163324 163330 163334 163336 163342 163346 163352 163360 203614
| A. | n=1 m=1 | B. | n=2 m=2 | C. | n=3 m=3 | D. | n=2 m=3 |
