题目内容
14.现有反应:xA(g)+yB(g)?zC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:(1)该反应的逆反应为放热反应,且x+y>z (填“>”“=”“<”).
(2)减压时,A的质量分数增大.(填“增大”“减小”或“不变”,下同)
(3)若加入B(保持体系体积不变),则A的转化率增大,B的转化率减小.
(4)若升高温度,则平衡时B、C的浓度之比$\frac{c(B)}{c(C)}$将减小.
(5)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色变深,而维持容器内压强不变,充入氖气时,混合物颜色变浅(填“变深”“变浅”或“不变”).
分析 达到平衡后,当升高温度时,B的转化率变大,说明温度升高平衡向正反应方向移动,则正反应吸热,当减小压强时,混合体系中C的质量分数也减小,说明压强减小平衡向逆反应方向移动,则方程式中反应物的气体的计量数之和大于生成物气体的化学计量数之和,根据外界条件对化学平衡的影响解答该题.
解答 解:(1)达到平衡后,当升高温度时,B的转化率变大,说明温度升高平衡向正反应方向移动,则正反应吸热,逆反应为放热反应,当减小压强时,混合体系中C的质量分数也减小,说明压强减小平衡向逆反应方向移动,则方程式中反应物的气体的计量数之和大于生成物气体的化学计量数之和,
故答案为:放;>;
(2)减压,平衡向着方程式中气体的计量数之和增大的反应方向移动,即向着逆反应方向移动,则A的质量分数增大,故答案为:增大;
(3)在反应容器中加入一定量的B,反应物B的浓度增大,平衡向正反应方向移动,则A的转化率增大,B的转化率减小,故答案为:增大;减小;
(4)正反应吸热,则升高温度平衡向正反应方向移动,B的物质的量减小,C的物质的量增多,所以二者的浓度比值将减小,故答案为:减小;
(5)B是有色物质,A、C均无色,则加入C(体积不变)时,平衡逆向移动,B的浓度增大,则混合物颜色变深;而维持容器内压强不变,充入氖气时,则体积增大,所以混合物颜色变浅,故答案为:变深;变浅.
点评 本题考查外界条件对平衡移动的影响,题目难度不大,注意分析反应的特征为解答该题的关键.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
4.下列有关说法正确的是( )
| A. | 蔗糖、淀粉、蛋白质、油脂都是营养物质,都属于高分子化合物,都能发生水解反应 | |
| B. | 人造纤维、合成纤维、碳纤维、光导纤维主要成分都是纤维素 | |
| C. | 乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 | |
| D. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
5.砷(As)元素与P元素同一主族,下列关于砷(As)元素的叙述不正确的是( )
| A. | 最高价氧化物的化学式为As2O5 | |
| B. | 气态氢化物的稳定性强于磷化氢而弱于硫化氢 | |
| C. | 砷单质在通常状况下为固态 | |
| D. | 砷酸是一种弱酸,酸性比磷酸酸性弱 |
2.元素的性质呈周期性变化的根本原因是( )
| A. | 元素的原子半径呈周期性变化 | |
| B. | 元素原子量的递增,量变引起质变 | |
| C. | 元素的金属性和非金属性呈周期性变化 | |
| D. | 元素原子的核外电子排布呈周期性变化 |
9.石墨和金刚石都是碳的单质,石墨在一定条件下可转化为金刚石.已知12g石墨完全转化成金刚石时,要吸收1.9kJ的能量.下列说法正确的是( )
| A. | 石墨不如金刚石稳定 | |
| B. | 由金刚石制备石墨是吸热反应 | |
| C. | 等质量的石墨与金刚石完全燃烧,金刚石放出的能量更多 | |
| D. | 等质量的石墨与金刚石完全燃烧,石墨放出的能量更多 |
19.江苏省已开始大力实施“清水蓝天”工程.下列不利于“清水蓝天”工程实施的是( )
| A. | 将废旧电池深埋,防止污染环境 | |
| B. | 加强城市生活污水脱氮除磷处理,遏制水体富营养化 | |
| C. | 积极推广太阳能、风能、地热能及水能等的使用,减少化石燃料的使用 | |
| D. | 大力实施矿物燃料“脱硫、脱硝技术”,减少硫的氧化物和氮的氧化物污染 |
6. 如图,利用培养皿探究氨气的性质.实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面.下列对实验现象所做的解释正确的是( )
如图,利用培养皿探究氨气的性质.实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面.下列对实验现象所做的解释正确的是( )
 如图,利用培养皿探究氨气的性质.实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面.下列对实验现象所做的解释正确的是( )
如图,利用培养皿探究氨气的性质.实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面.下列对实验现象所做的解释正确的是( )| A. | 浓盐酸附近产生白烟:NH3与HCl气体反应产生了NH4Cl固体 | |
| B. | 浓硫酸附近无明显现象:NH3与浓硫酸不发生反应 | |
| C. | 氯化物溶液变浑浊:该溶液一定是AlCl3溶液 | |
| D. | 湿润的红色石蕊试纸变蓝:NH3的水溶液显碱性 |
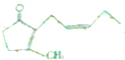 ),其香味浓郁,被广泛应用于化妆品的制造中.
),其香味浓郁,被广泛应用于化妆品的制造中.