题目内容
18.图中化合物B既能使溴水褪色,又能溶解碳酸钙,D、E均为高分子化合物.根据如图填空: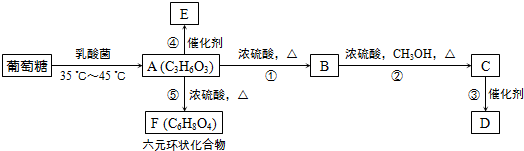
(1)写出葡萄糖与新制氢氧化铜浊液反应的化学方程式:CH2OH(CHOH)4CHO+2Cu(OH)2$\stackrel{△}{→}$CH2OH(CHOH)4COOH+Cu2O↓+2H2O.
(2)A中的官能团有-OH,-COOH(写结构简式).
(3)E在自然界中可降解,对环境无害,下列说法正确的是ad.
a.E是一种线型高分子 b.由A生成E的反应属于加聚反应
c.E的相对分子质量为72 d.E用作一次性快餐盒有助于减少白色污染
(4)在反应 ①~⑤中,属于取代反应的是②⑤.写出反应③和⑤的化学方程式:③nCH2=CHCOOCH3$\stackrel{催化剂}{→}$
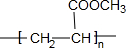 ,⑤2
,⑤2 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +2H2O.
+2H2O.(5)A跟氢氧化钙作用可制得一种常用的人体补钙剂,测得这种补钙剂的纯净物中钙元素的质量分数为13.0%,其结晶水的含量为29.2%.
分析 葡萄糖在乳酸菌作用下生成乳酸,A为 ,乳酸通过缩聚反应生成高分子化合物E,化合物B既能使溴水褪色,又能溶解碳酸钙,说明B为CH2=CHCOOH,A→B为消去反应,B与甲醇发生酯化反应生成的C为CH2=CHCOOCH3,C发生加聚反应生成高分子化合物D,乳酸通过分子间酯化生成环状化合物F,据此分析.
,乳酸通过缩聚反应生成高分子化合物E,化合物B既能使溴水褪色,又能溶解碳酸钙,说明B为CH2=CHCOOH,A→B为消去反应,B与甲醇发生酯化反应生成的C为CH2=CHCOOCH3,C发生加聚反应生成高分子化合物D,乳酸通过分子间酯化生成环状化合物F,据此分析.
解答 解:(1)葡萄糖中含有醛基,能够被新制氢氧化铜氧化为羧基,化学方程式为,CH2OH(CHOH)4CHO+2Cu(OH)2$\stackrel{△}{→}$ CH2OH(CHOH)4COOH+Cu2O↓+2H2O,
故答案为:CH2OH(CHOH)4CHO+2Cu(OH)2$\stackrel{△}{→}$ CH2OH(CHOH)4COOH+Cu2O↓+2H2O;
(2)葡萄糖在乳酸菌作用下生成乳酸,A为 ,含有羟基和羧基,故答案为:-OH,-COOH;
,含有羟基和羧基,故答案为:-OH,-COOH;
(3)乳酸通过缩聚反应生成高分子化合物E,E在自然界中可降解,对环境无害,所以ad正确,bc错误,故答案为:ad;
(4)反应①为消去反应,②酯化反应即取代反应,③为加聚反应,化学方程式为nCH2=CHCOOCH3$\stackrel{催化剂}{→}$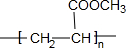 ,④为缩聚反应,⑤为酯化反应即取代反应,反应方程式为2
,④为缩聚反应,⑤为酯化反应即取代反应,反应方程式为2 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +2H2O,
+2H2O,
故答案为:②⑤;nCH2=CHCOOCH3$\stackrel{催化剂}{→}$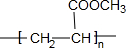 ;2
;2 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +2H2O;
+2H2O;
(5)设乳酸钙中水的含量为x,则其分子式为CaC6H10O6•xH2O,钙元素的质量分数为13.0%,则有$\frac{40}{40+12×6+1×10+16×6+18x}$×100%=13%,x=5,$\frac{5×18}{40+12×6+1×10+16×6+5×18}$×100%=29.2%,故答案为:29.2%.
点评 本题考查有机推断,题目难度较大,题目信息反应原理为解答关键,注意掌握常见有机物结构与性质,明确乳酸结构,试题侧重考查学生灵活应用基础知识的能力.

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案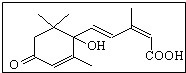 国庆期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,下列关于该物质的说法正确的是( )
国庆期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,下列关于该物质的说法正确的是( )| A. | 其分子式为C15H18O4 | |
| B. | 分子中存在4种含氧官能团 | |
| C. | 既能发生加聚反应,又能发生缩聚反应 | |
| D. | 1mol该有机物最多可与3molH2发生加成反应 |

| A. | 水杨酸和茉莉醛均能发生银镜反应 | |
| B. | 乙酰水杨酸可以由水杨酸发生酯化反应生成 | |
| C. | 四种有机物都含有碳碳双键,都能和氢气发生加成反应 | |
| D. | 四种机物中只有乙酰水杨酸能发生水解反应 |
| 乙 | 丙 | 丁 | |
| 甲 | 戊 |
(2)原子半径:甲>丁(填“<”、“>”或“=”);
(3)元素的非金属性:甲<丙(填“<”、“>”或“=”).
①开发太阳能、风能和氢能等能源
②大量开采地下水,以满足生产、生活的需求
③使用布袋购物、以步代车等属于“低碳生活”方式
④开发利用可燃冰是缓解能源紧缺的唯一途径
⑤利用可降解的“玉米塑料”生产一次性饭盒.
| A. | ①③⑤ | B. | ①②③ | C. | ②④⑤ | D. | ①②④ |
| A. | “另一种反应物”在反应中表现还原性 | |
| B. | CuH在化学反应中既可做氧化剂也可做还原剂 | |
| C. | CuH在氯气中燃烧的化学方程式为CuH+Cl2$\frac{\underline{\;点燃\;}}{\;}$CuCl+HCl | |
| D. | CuH与盐酸反应生成的气体是H2 |

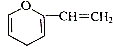
 、
、 、
、 ;
;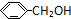 ;
;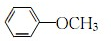 .
.