题目内容
【题目】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中。“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如下:
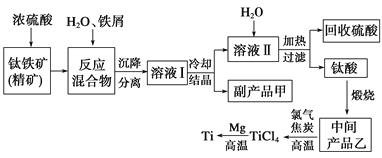
已知反应:①将钛铁矿与浓H2SO4煮解:FeTiO3+2H2SO4(浓) ![]() TiOSO4(硫酸氧钛)+FeSO4+2H2O。②加水热分解硫酸氧钛:TiOSO4+(n+1)H2O
TiOSO4(硫酸氧钛)+FeSO4+2H2O。②加水热分解硫酸氧钛:TiOSO4+(n+1)H2O![]() TiO2·nH2O+H2SO4。
TiO2·nH2O+H2SO4。
请回答下列问题:
(1)副产品甲是____________,可循环利用的物质是___________________________。
(2)上述生产流程中加入铁屑的目的是_______________________________________。
(3)写出中间产品乙与焦炭、氯气在高温下发生反应的方程式为:________________。
(4)“硫酸法”生产钛排放的废液对水体有哪些污染,请指出主要的两点:
①_________________________________;②_______________________________。
针对其中一项污染,提出处理的方法: 。
【答案】 FeSO4·7H2O(名称、俗名亦可) 硫酸(H2SO4) 防止Fe2+被氧化(合理答案均计分) TiO2+2Cl2+2C![]() TiCl4+2CO(写CO2也给分) 酸污染、重金属离子(Cu2+、Cr3+等)污染(合理答案均计分) 中和法、沉淀法(合理答案均计分)
TiCl4+2CO(写CO2也给分) 酸污染、重金属离子(Cu2+、Cr3+等)污染(合理答案均计分) 中和法、沉淀法(合理答案均计分)
【解析】试题分析:(1)从流程图可知铁元素进入副产品甲,硫酸与过量的铁反应生成FeSO4,可循环利用的物质是硫酸。
(2)生产流程中加入铁屑的目的是防止Fe2+被氧化; (3)钛酸灼烧生成二氧化钛和水,二氧化钛与焦炭、氯气在高温下发生反应生成TiCl4和CO;
(4)“硫酸法”生产钛排放的废液是酸性,会产生酸污染;与Ti共存的其它重金属的废液对水体有污染。
解析:(1) 从流程图可知铁元素进入副产品甲,硫酸与过量的铁反应生成FeSO4,副产品甲是FeSO4·7H2O,可循环利用的物质是硫酸。
(2)生产流程中加入铁屑的目的是防止Fe2+被氧化;
(3)钛酸灼烧生成二氧化钛和水,二氧化钛与焦炭、氯气在高温下发生反应生成TiCl4和CO,反应方程式为TiO2+2Cl2+2C![]() TiCl4+2CO;
TiCl4+2CO;
(4)“硫酸法”生产钛排放的废液是酸性,会产生酸污染;与Ti共存的其它重金属的废液对水体有污染,处理的方法硫酸用石灰中和的方法、重金属离子污染可通过沉淀法除去。

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案【题目】(Ⅰ)(1)用系统命名法给下列有机物命名或写出对应的结构简式。
① _________________
_________________
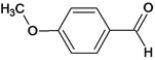
②![]() _________________
_________________
③1,3,5—三甲苯_________________
(Ⅱ)某工厂废液经测定得知主要含有乙醇,其中还有丙酮和乙酸。根据下表中各物质的性质,按下列步骤回收乙醇和乙酸.
物质 | 丙酮 | 乙醇 | 乙酸 |
沸点/℃ | 56.2 | 78.5 | 117.9 |
①向废液中加入烧碱溶液,调整溶液的pH=10;
②将混合液放入蒸馏器中缓缓加热;
③收集温度在70℃~85℃时的馏出物;
④排出蒸馏器中的残液,冷却后向其中加浓硫酸(过量),然后再放入耐酸蒸馏器中进行蒸馏,回收馏出物。
请回答下列问题:
(2)加入烧碱使溶液的pH=10的目的是___________________。
(3)在70℃~85℃时馏出物的主要成分是__________________。
(4)黄酮类药物中部分化合物具有很好的药用价值,比如可以降低血管的脆性,改善血管的通透性、降低血脂和胆固醇,用于防治老年高血压和脑溢血。酮类化合物A是黄酮类药物的一中合成中间体,其结构如下:
化合物A的同分异构体中,既能发生银镜反应,又能与FeCl3溶液发生显色反应的共有_______种(已知:酚羟基能与FeCl3溶液发生显色反应,醛基可发生银镜反应),其中核磁共振氢谱为5组峰,且峰面积为2:2:2:1:1的为:_____________