题目内容
【题目】下表是元素周期表的一部分, 针对表中的①~⑧种元素,填写下列空白:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA[ | 零 |
2 | ① | ② | ③ | |||||
3 | ④[ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)上述元素中,化学性质最不活泼的是 (填元素符号)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是 (填元素符号)。
(3)元素②的气态氢化物分子属于 (填电解质或非电解质);元素⑦与④形成化合物的电子式是 。
(4)元素⑤的最高价氧化物与氢氧化钠溶液反应的离子方程式为: 。
(5)元素④的某氧化物可作供氧剂,该氧化物中所含的化学键类型有 ,写出其与二氧化碳反应的化学方程式 。
【答案】(每空2分,共14分)
(1)Ar
(2)HClO4
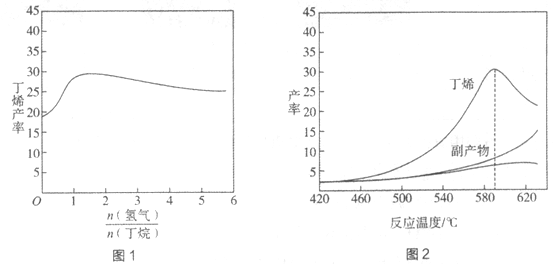
(3)非电解质;![]()
(4)Al2O3+ 2OH—= H2O + 2AlO2—
(5)离子键、共价键;2Na2O2+ 2CO2= 2Na2CO3+ O2↑
【解析】
试题由元素在周期表中位置,可知①为C、②为N、③为O、④为Na、⑤为Al、⑥为Si、⑦为Cl、⑧为Ar。
(1)稀有气体Ar的化学性质最不活泼,则化学性质最不活泼的为Ar。
故答案为:Ar;
(2)以上元素中,最高价氧化物对应水化物的酸性最强的为高氯酸,化学式为HClO4。
故答案为:HClO4;
(3)②的氢化物为NH3,氨气为非电解质;元素⑦与④形成化合物为NaCl,氯化钠为离子化合物,其电子式为:![]() 。
。
故答案为:非电解质;![]() ;
;
(4)⑤为Al元素,其最高价氧化物为氧化铝,氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,反应的离子方程式为:Al2O3+2OH-=H2O+2AlO2-。
故答案为:Al2O3+2OH-=H2O+2AlO2-;
(5)元素④的某氧化物可作供氧剂,该氧化物为过氧化钠,过氧化钠中所含的化学键类型有离子键和共价键;过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应方程式为:2Na2O2+2CO2=2Na2CO3+O2。
故答案为:离子键、共价键;2Na2O2+2CO2=2Na2CO3+O2。

【题目】在l0℃时,10 mL 0.4 mol L-1H2O2溶液发生催化分解:2H2O2![]() 2H2O+O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表:
2H2O+O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表:
t/min | 0 | 2 | 4 | 6 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 |
下列叙述不正确的是(溶液体积变化忽略不计)
A. 0~2 min的平均反应速率比4~6 min快
B. 0~6 min 的平均反应速率v(H2O2)=3.3×10-2 moL-1 L-1 min-1
C. 反应至 6 min 时,c(H2O2)=0.3 mol·L-1
D. 反应至6 min时,H2O2分解了50%