题目内容
某温度时,用等体积的乙醇和乙酸反应生成酯。开始时,乙醇的物质量浓度为2摩/升,乙酸的物质的量浓度为4摩/升。达到平衡时,85%的乙醇参加了反应,这时溶液中乙酸的物质的量浓度约为 ( )
A.3.4摩/升 B.2.3摩/升 C.1.7摩/升 D.1.15摩/升
【答案】
D
【解析】
试题分析:设溶液的体积都是1L,则乙醇和乙酸的物质的量分别是2mol和4mol。其中参加反应的乙醇是2mol×85%=1.7mol,因此根据化学方程式可知,消耗乙酸的物质的量也是1.7mol,所以剩余乙酸的物质的量是4mol-1.7mol=2.3mol。由于溶液的体积变为2L,因此乙酸的浓度是2.3mol÷2L=1.15mol/L,答案选D。
考点:考查酯化反应的有关计算
点评:该题难度不大,侧重对学生能力的考查。该题主要是根据反应的化学方程式列式计算即可,需要注意的是反应后的溶液体积不是1L,而是2L,否则会得出错误的答案。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
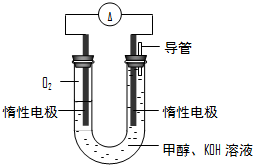 (2013?上饶一模)“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题
(2013?上饶一模)“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题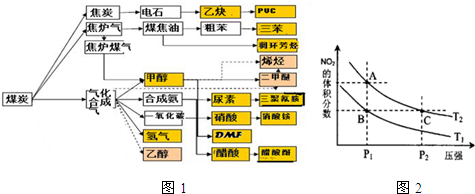
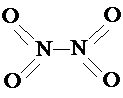 .已知N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式为
.已知N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式为 Ag+(aq)+Cl-(aq)在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水 ②100 mL
0.3 mol·L-1 AgNO3溶液
③100 mL 0.1 mol·L-1MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为
(填序号),此时溶液②中Cl-物质的量浓度为
。
Ag+(aq)+Cl-(aq)在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水 ②100 mL
0.3 mol·L-1 AgNO3溶液
③100 mL 0.1 mol·L-1MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为
(填序号),此时溶液②中Cl-物质的量浓度为
。