题目内容
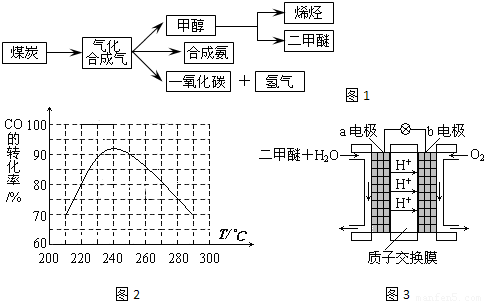
如图1是煤化工产业链的一部分,试运用所学知识,解决下列问题:
(1)该产业链中合成氨的反应在较低温下能否自发进行?
(2)已知该产业链中某反应的平衡表达式为:K=
,它所对应的化学反应为:
(3)已知在一定温度下,各反应的平衡常数如下:
C(s)+CO2(g)?2CO(g),K1
CO(g)+H2O(g?H2(g)+CO2(g),K2
C(s)+H2O(g)?CO(g)+H2(g),K3
则K1、K2、K3之间的关系是:
(4)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
该反应的正反应方向是
(5)从图中看出氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是 和
和 .已知N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式为
.已知N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式为
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
(6)以上述产业链中甲醇为燃料制成燃料电池,请写出在氢氧化钾介质中该电池的负极反应式

(1)该产业链中合成氨的反应在较低温下能否自发进行?
可以
可以
.(2)已知该产业链中某反应的平衡表达式为:K=
| C(H2)C(CO) |
| C(H2O) |
C(s)+H2O(g)?CO(g)+H2(g);
C(s)+H2O(g)?CO(g)+H2(g);
.(3)已知在一定温度下,各反应的平衡常数如下:
C(s)+CO2(g)?2CO(g),K1
CO(g)+H2O(g?H2(g)+CO2(g),K2
C(s)+H2O(g)?CO(g)+H2(g),K3
则K1、K2、K3之间的关系是:
K3=K1×K2
K3=K1×K2
.(4)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
放热
放热
反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,CO的平衡转化率为:75%
75%
.(5)从图中看出氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是
 .已知N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式为
.已知N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式为2NO2(g)?N2O4(g)△H=-57kJ?mol-1
2NO2(g)?N2O4(g)△H=-57kJ?mol-1
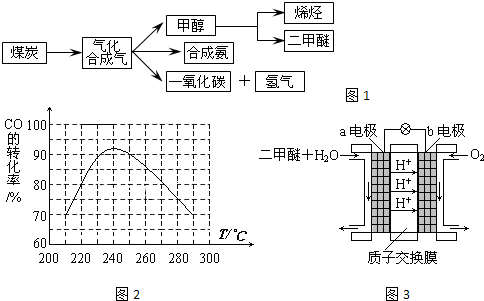
.对反应N2O4(g)?2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.下列说法正确的是D
D
.A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
(6)以上述产业链中甲醇为燃料制成燃料电池,请写出在氢氧化钾介质中该电池的负极反应式
CH3OH+8OH--6e-═CO32-+6H2O;
CH3OH+8OH--6e-═CO32-+6H2O;
.分析:(1)生产氨气的反应放出大量的热,△H<0,△S<O,△G=△H-T△S<0能自发进行;
(2)根据平衡常数的定义判断反应的方程式,注意固体和纯液体不在表达式中;
(3)根据平衡常数的表达式推断;
(4)根据温度变化平衡常数的变化判断温度对化学平衡移动的影响,进而判断反应热,利用三段式法计算转化率;
(5)根据反应热等于反应物的总键能减去生成物的总键能计算反应热,从平衡移动的角度分析各物理量的变化;
(6)甲醇具有还原性,在负极上发生氧化反应生成碳酸根离子,以此书写电极反应式.
(2)根据平衡常数的定义判断反应的方程式,注意固体和纯液体不在表达式中;
(3)根据平衡常数的表达式推断;
(4)根据温度变化平衡常数的变化判断温度对化学平衡移动的影响,进而判断反应热,利用三段式法计算转化率;
(5)根据反应热等于反应物的总键能减去生成物的总键能计算反应热,从平衡移动的角度分析各物理量的变化;
(6)甲醇具有还原性,在负极上发生氧化反应生成碳酸根离子,以此书写电极反应式.
解答:解:(1)生产氨气的反应:N2+3H2?2NH3放出大量的热,△H<0,△S<O,所以在低温下易进行△G=△H-T△S<0能自发进行,故答案为:可以;
(2)平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积,平衡常数中,分子为生成物,分母为反应物,所以该反应的方程式为:C(s)+H2O(g)?CO(g)+H2(g),
故答案为:C(s)+H2O(g)?CO(g)+H2(g);
(3)根据化学方程式可知:K1=
,K2=
,K3=
,
所以K3=
×
=
=K1×K2,
故答案为:K3=K1×K2;
(4)由表中数据可知,随着温度的升高,平衡常数减小,说明升高温度平衡向逆反应方向移动,说明正反应为让热反应,设平衡时转化的CO为xmol/L,
利用三段式法计算:
CO(g)+H2O(g)?H2(g)+CO2(g),
起始(mol/L):0.020 0.020 0 0
转化(mol/L):x x x x
平衡(mol/L):0.02-x 0.02-x x x
则有K
=
=9
解之得:x=0.015,
所以转化率为
×100%=75%,
故答案为:放热,75%;
(5)反应热等于反应物的总键能减去生成物的总键能,则反应热为:△H=-2×2×466KJ/mol-(167KJ/mol+4×438.5KJ/mol)=-57KJ/mol,反应的热化学方程式为:2NO2(g)?N2O4(g)△H=-57 kJ?mol-1;
对于反应N2O4(g)?2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.则
A.A点压强小于C点的压强,压强越大,反应速率越大,则反应速率:A<C,故A错误;
B.增大压强,平衡向正反应移动,但浓度的增大幅度大于转化的程度,所以C点浓度大,颜色深,故B错误;
C.B、C两点二氧化氮的体积分数相同,则混合气体的平均相对分子质量相同,故C错误;
D.在相同压强下,升高温度,平衡向逆反应方向移动,则二氧化氮的体积分数增大,所以由状态B到状态A,可以用加热的方法,故D正确,
故答案为:2NO2(g)?N2O4(g)△H=-57 kJ?mol-1; D;
(6)甲醇具有还原性,在负极上发生氧化反应生成碳酸根离子,反应的电极反应式为:CH3OH+8OH--6e-═CO32-+6H2O,
故答案为:CH3OH+8OH--6e-═CO32-+6H2O;
(2)平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积,平衡常数中,分子为生成物,分母为反应物,所以该反应的方程式为:C(s)+H2O(g)?CO(g)+H2(g),
故答案为:C(s)+H2O(g)?CO(g)+H2(g);
(3)根据化学方程式可知:K1=
| c2(CO) |
| c(CO2) |
| c(H2)×c(CO2) |
| c(CO)×c(H2O) |
| c(CO)×c(H2) |
| c(H2O) |
所以K3=
| c(H2)×c(CO2) |
| c(CO)×c(H2O) |
| c2(CO) |
| c(CO2) |
| c(CO)×c(H2) |
| c(H2O) |
故答案为:K3=K1×K2;
(4)由表中数据可知,随着温度的升高,平衡常数减小,说明升高温度平衡向逆反应方向移动,说明正反应为让热反应,设平衡时转化的CO为xmol/L,
利用三段式法计算:
CO(g)+H2O(g)?H2(g)+CO2(g),
起始(mol/L):0.020 0.020 0 0
转化(mol/L):x x x x
平衡(mol/L):0.02-x 0.02-x x x
则有K
| c(H2)×c(CO2) |
| c(CO)×c(H2O) |
| x?x |
| (0.020-x)?(0.020-x) |
解之得:x=0.015,
所以转化率为
| 0.015mol/L |
| 0.02mol/L |
故答案为:放热,75%;
(5)反应热等于反应物的总键能减去生成物的总键能,则反应热为:△H=-2×2×466KJ/mol-(167KJ/mol+4×438.5KJ/mol)=-57KJ/mol,反应的热化学方程式为:2NO2(g)?N2O4(g)△H=-57 kJ?mol-1;
对于反应N2O4(g)?2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.则
A.A点压强小于C点的压强,压强越大,反应速率越大,则反应速率:A<C,故A错误;
B.增大压强,平衡向正反应移动,但浓度的增大幅度大于转化的程度,所以C点浓度大,颜色深,故B错误;
C.B、C两点二氧化氮的体积分数相同,则混合气体的平均相对分子质量相同,故C错误;
D.在相同压强下,升高温度,平衡向逆反应方向移动,则二氧化氮的体积分数增大,所以由状态B到状态A,可以用加热的方法,故D正确,
故答案为:2NO2(g)?N2O4(g)△H=-57 kJ?mol-1; D;
(6)甲醇具有还原性,在负极上发生氧化反应生成碳酸根离子,反应的电极反应式为:CH3OH+8OH--6e-═CO32-+6H2O,
故答案为:CH3OH+8OH--6e-═CO32-+6H2O;
点评:本题考查较为综合,涉及知识点较多,难度较大,易错点为(1),根据△G=△H-T△S<0能自发进行.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
如图1是煤化工产业链的一部分,试运用所学知识,解决下列问题:
(1)该产业链中合成氨的反应在较低温下能否自发进行? .
(2)已知该产业链中某反应的平衡表达式为: ,它所对应的化学反应为: .
,它所对应的化学反应为: .
(3)已知在一定温度下,各反应的平衡常数如下:
C(s)+CO2(g)?2CO(g),K1
CO(g)+H2O(g?H2(g)+CO2(g),K2
C(s)+H2O(g)?CO(g)+H2(g),K3
则K1、K2、K3之间的关系是: .
(4)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
该反应的正反应方向是 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,CO的平衡转化率为: .
(5)从图中看出氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是 和
和 .已知N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式为 .对反应N2O4(g)?2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.下列说法正确的是 .
.已知N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式为 .对反应N2O4(g)?2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.下列说法正确的是 .
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
(6)以上述产业链中甲醇为燃料制成燃料电池,请写出在氢氧化钾介质中该电池的负极反应式 .

(1)该产业链中合成氨的反应在较低温下能否自发进行? .
(2)已知该产业链中某反应的平衡表达式为:
 ,它所对应的化学反应为: .
,它所对应的化学反应为: .(3)已知在一定温度下,各反应的平衡常数如下:
C(s)+CO2(g)?2CO(g),K1
CO(g)+H2O(g?H2(g)+CO2(g),K2
C(s)+H2O(g)?CO(g)+H2(g),K3
则K1、K2、K3之间的关系是: .
(4)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(5)从图中看出氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
(6)以上述产业链中甲醇为燃料制成燃料电池,请写出在氢氧化钾介质中该电池的负极反应式 .

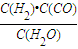 ,它所对应反应的化学方程式为______.
,它所对应反应的化学方程式为______.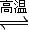 CH3OH(g)△H1=-90.7kJ?mol-1
CH3OH(g)△H1=-90.7kJ?mol-1 CH3OCH3(g)+H2O(g)△H2=-23.5kJ?mol-1
CH3OCH3(g)+H2O(g)△H2=-23.5kJ?mol-1 CO2(g)+H2(g)△H3=-41.2kJ?mol-1
CO2(g)+H2(g)△H3=-41.2kJ?mol-1