题目内容
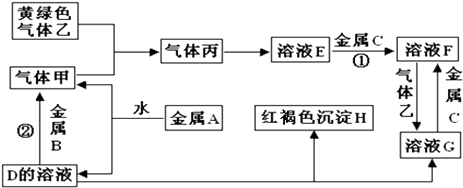
【题目】已知A、B、C、D是中学化学的常见物质,它们在一定条件下有如下转化关系:A ![]() B
B ![]() C
C
(1)若A为能使湿润的红色石蕊试纸变蓝的气体,C为红棕色气体.则A的空间构型为 , A转化为B反应的化学方程式为 .
(2)若A、B、C均为氧化物,A为砖红色固体,且A中金属元素为+1价,D是一种黑色固态非金属单质,则A的化学式为 , B的电子式为 .
(3)若D为氯碱工业的主要产品,B为高中常见的一种具有两性的物质,则C溶液中除氢氧根外还存在的阴离子的化学式为 . 氯碱工业中阴极的电极反应式为 .
【答案】
(1)三角锥形;4NH3+5O2 ![]() ?4NO+6H2O
?4NO+6H2O
(2)Cu2O;![]()
(3)[Al(OH)4]﹣;2H++2e﹣=H2↑或2H2O+2 e﹣=H2↑+2OH﹣
【解析】解:(1)若A为能使湿润的红色石蕊试纸变蓝的气体,则A为NH3 , 红棕色气体C为NO2 , D为氧气,B为NO,该过程为氨气的连续氧化反应,NH3为三角锥形结构,A转化为B反应的化学方程式为:4NH3+5O2 ![]() 4NO+6H2O, 所以答案是:三角锥形;4NH3+5O2
4NO+6H2O, 所以答案是:三角锥形;4NH3+5O2 ![]() 4NO+6H2O;(2)若A、B、C均为氧化物,A为砖红色固体,且A中金属元素为+1价,A为Cu2O,D是一种黑色固态非金属单质,则D为C,B是CO2 , C是CO,二氧化碳的电子式为:
4NO+6H2O;(2)若A、B、C均为氧化物,A为砖红色固体,且A中金属元素为+1价,A为Cu2O,D是一种黑色固态非金属单质,则D为C,B是CO2 , C是CO,二氧化碳的电子式为: ![]() ,
,
所以答案是:Cu2O; ![]() ;(3)若D为氯碱工业的主要产品,B为高中常见的一种具有两性的物质,A是NaOH,B为Al(OH)3 , A是Al3+ , C是[Al(OH)4]﹣ , 氯碱工业中阴极的电极反应式为:2H++2e﹣=H2↑或2H2O+2 e﹣=H2↑+2OH﹣ ,
;(3)若D为氯碱工业的主要产品,B为高中常见的一种具有两性的物质,A是NaOH,B为Al(OH)3 , A是Al3+ , C是[Al(OH)4]﹣ , 氯碱工业中阴极的电极反应式为:2H++2e﹣=H2↑或2H2O+2 e﹣=H2↑+2OH﹣ ,
所以答案是:[Al(OH)4]﹣;2H++2e﹣=H2↑或2H2O+2 e﹣=H2↑+2OH﹣ .