ћвƒњƒЏ»Ё
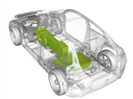
°Њћвƒњ°њ“ї÷÷–¬–Ќµƒ““іЉµз≥Ў£®DEFC£© «”√ї«Ћбја÷ „”»№ЉЅ„чµзљв÷ £ђ‘Џ 200°ж„у”“ ±є©µз£® »з ѕ¬ ЌЉ Ћщ Њ £©£ђ ±» Љ„ іЉ µз ≥Ў –І ¬ Єя ≥ц 32 ±ґ £ђ «“ ±» љѕ ∞≤ »Ђ °£ µз ≥Ў „№ Јі ”¶ ќ™C2H5OH+3O2==2CO2+3H2O°£‘тѕ¬Ѕ–ЋµЈ®’э»Јµƒ «£® £©
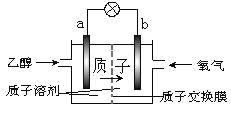
A.a ЉЂќ™µз≥Ўµƒ’эЉЂ
B.µз≥Ў’эЉЂµƒµзЉЂЈі”¶£ЇO2 + 4H+ + 4e- = 2H2O
C.µз≥Ўє§„ч ±µз„””… b ЉЂ—ЎµЉѕяЊ≠µ∆≈Ё‘ўµљ a ЉЂ
D.»№“Ї÷– H+ ѕт a µзЉЂ“∆ґѓ
°Њір∞Є°њB
°Њљвќц°њ
”…÷ „”µƒґ®ѕт“∆ґѓњ…÷™aќ™ЄЇЉЂ£ђbќ™’эЉЂ£ђЄЇЉЂЈҐ…ъ—хїѓЈі”¶£ђ““іЉ±ї—хїѓ…ъ≥…CO2ЇЌ£ђµзЉЂЈі”¶ љќ™C2H5OH+3H2O-12e-=2CO2+12H+£ђ’эЉЂ—х∆шµ√µљµз„”±їїє‘≠£ђµзЉЂЈі”¶ љќ™4H++O2+4e-=2H2O£ђљбЇѕµзЉЂЈі”¶љвірЄ√ћв°£
A£ЃЄщЊЁ÷ „”“∆ґѓЈљѕт÷™£ђa «ЄЇЉЂ£ђb «’эЉЂ£ђє Aінќу£ї
B£Ѓ’эЉЂ…ѕ—х∆шµ√µз„”ЇЌ«вјл„”Јі”¶…ъ≥…ЋЃ£ђµзЉЂЈі”¶ љќ™4H++O2+4e-=2H2O£ђє B’э»Ј£ї
C£Ѓa «ЄЇЉЂ£ђb «’эЉЂ£ђЄЇЉЂ…ѕ Іµз„”ЈҐ…ъ—хїѓЈі”¶£ђ’эЉЂ…ѕµ√µз„”ЈҐ…ъїє‘≠Јі”¶£ђ‘тµз„”і”ЄЇЉЂ—ЎµЉѕяЅчѕт’эЉЂ£ђє Cінќу£ї
D£Ѓµз≥Ўє§„ч ±£ђ»№“Ї÷– H+ѕт’эЉЂ£ђЉіbµзЉЂ“∆ґѓ£ђє Dінќу£ї
є ір∞Єќ™A°£

 њ™–ƒњмј÷Љў∆Џ„ч“µ оЉў„ч“µќч∞≤≥ц∞ж…зѕµЅ–ір∞Є
њ™–ƒњмј÷Љў∆Џ„ч“µ оЉў„ч“µќч∞≤≥ц∞ж…зѕµЅ–ір∞Є √ыћв—µЅЈѕµЅ–ір∞Є
√ыћв—µЅЈѕµЅ–ір∞Є°Њћвƒњ°њѕ¬Ѕ–ƒ№Ѕњ„™їѓєэ≥ћ”л—хїѓїє‘≠Јі”¶ќёєЎµƒ «
A. єићЂ—фƒ№µз≥Ў | B. пЃјл„”µз≥ЎЈ≈µз | C. їрЉэµƒ»ЉЅѕ»Љ…’ | D. ∆ѕћ—ћ«ћбє©ƒ№Ѕњ |
|
|
|
|
A. A B. B C. C D. D
°Њћвƒњ°њt °ж ±£ђ‘Џ»Ёїэ≤ї±дµƒ√№±’»Ё∆ч÷–ЈҐ…ъЈі”¶X(g)£Ђ3Y(g) ![]() 2Z(g)£ђЄч„йЈ÷‘Џ≤їЌђ ±њћµƒ≈®ґ»»з±нЋщ Њ£ђѕ¬Ѕ–ЋµЈ®’э»Јµƒ «(°°°°)
2Z(g)£ђЄч„йЈ÷‘Џ≤їЌђ ±њћµƒ≈®ґ»»з±нЋщ Њ£ђѕ¬Ѕ–ЋµЈ®’э»Јµƒ «(°°°°)
ќп÷ | X | Y | Z |
≥х Љ≈®ґ»/(mol°§L£≠1) | 0.1 | 0.2 | 0 |
2 min ±≈®ґ»/(mol°§L£≠1) | 0.08 | a | b |
∆љЇв≈®ґ»/(mol°§L£≠1) | 0.05 | 0.05 | 0.1 |
A.∆љЇв ±£ђXµƒ„™їѓ¬ ќ™20%
B.t °ж ±£ђЄ√Јі”¶µƒ∆љЇв≥£ эќ™40
C.∆љЇвЇу£ђ‘ціућеѕµ—є«њ£ђv’э‘ціу£ђvƒжЉх–°£ђ∆љЇвѕт’эЈі”¶Јљѕт“∆ґѓ
D.«∞2 minƒЏ£ђ”√Yµƒ±дїѓЅњ±н Њµƒ∆љЊщЈі”¶Ћў¬ v(Y)£љ0.03 mol°§L£≠1°§min£≠1
°Њћвƒњ°њN2O5 «“ї÷÷–¬–ЌѕхїѓЉЅ£ђ“їґ®ќ¬ґ»ѕ¬ЈҐ…ъ2N2O5(g)![]() 4NO2(g)£ЂO2(g)°°¶§H>0£ђT1ќ¬ґ»ѕ¬µƒ≤њЈ÷ µ—й эЊЁќ™
4NO2(g)£ЂO2(g)°°¶§H>0£ђT1ќ¬ґ»ѕ¬µƒ≤њЈ÷ µ—й эЊЁќ™
t/s | 0 | 500 | 1 000 | 1 500 |
c(N2O5)mol/L | 5.00 | 3.52 | 2.50 | 2.50 |
ѕ¬Ѕ–ЋµЈ®≤ї’э»Јµƒ «£® £©
A. 500 sƒЏN2O5Ј÷љвЋў¬ ќ™2.96°Ѕ10£≠3 mol/(L°§s)
B. T1ќ¬ґ»ѕ¬µƒ∆љЇв≥£ эќ™K1£љ125£ђ1 000 s ±„™їѓ¬ ќ™50%
C. ∆дЋыћхЉю≤ї±д ±£ђT2ќ¬ґ»ѕ¬Јі”¶µљ1 000 s ±≤вµ√N2O5(g)≈®ґ»ќ™2.98 mol/L£ђ‘тT1<T2
D. T1ќ¬ґ»ѕ¬µƒ∆љЇв≥£ эќ™K1£ђT2ќ¬ґ»ѕ¬µƒ∆љЇв≥£ эќ™K2£ђ»фT1>T2£ђ‘тK1>K2