题目内容
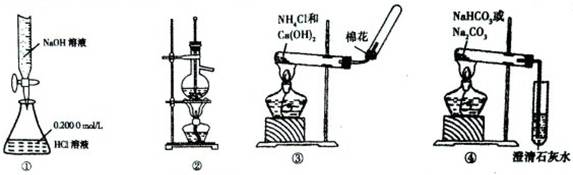
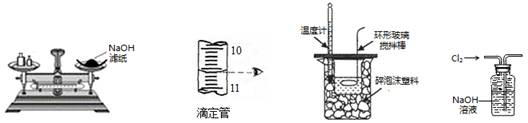
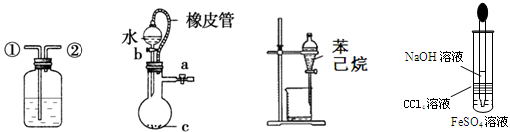
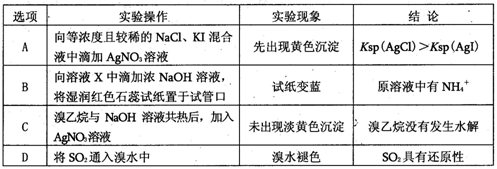
根据下列实验操作和现象所得出的结论不正确的是

C
试题分析:A、碘化银比氯化银更难溶,所以先出现黄色沉淀,说明氯化银的溶度积大于碘化银的溶度积,正确;B、能使湿润红色石蕊试纸变蓝的气体一定是氨气,所以与氢氧化钠溶液反应能产生氨气的溶液中一定含有铵根离子,正确;C、溴乙烷在氢氧化钠的水溶液中应发生水解反应,未出现淡黄色沉淀的原因是未加硝酸中和溶液中的氢氧化钠而造成的,不能证明溴乙烷没发生水解反应,错误;D、二氧化硫与溴水发生氧化还原反应而使溴水褪色,说明二氧化硫具有还原性,正确,答案选C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目