题目内容
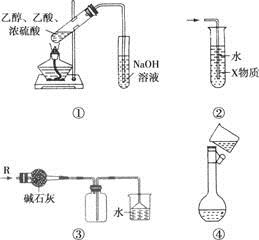
下列装置能达到实验目的是( )
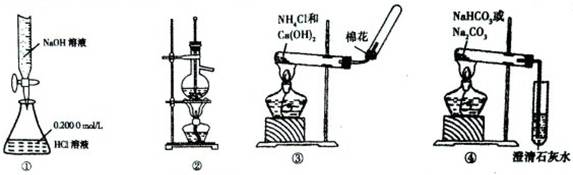

| A.用图①所示装置测定NaOH的浓度 | B.用图②所示装置分馏少量石油 |
| C.用图③所示装置在实验室制备收集氨气 | D.用图④所示装置鉴别碳酸钠和碳酸氢钠 |
D
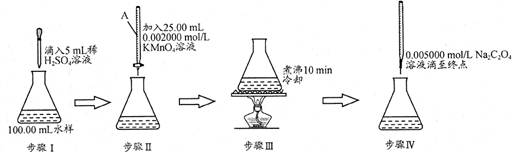
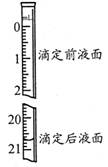
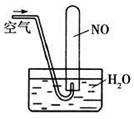
试题分析:A.滴定管不能伸入到锥形瓶中。错误。B.分馏少量石油时温度计的水银球的位置要在蒸馏烧瓶的支管口附近。错误。C。在实验室中用加热NH4Cl与Ca(OH)2固体混合物的方法制取氨气,用向下排空气法收集时导气管应该伸入到试管的底部。错误。D.NaHCO3不稳定,受热容易分解产生CO2使澄清的石灰水变浑浊,而Na2CO3受热不分解,因此可以用图④所示装置鉴别碳酸钠和碳酸氢钠。制取。

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
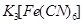 溶液,可看到Fe电极附近有蓝色沉淀生成
溶液,可看到Fe电极附近有蓝色沉淀生成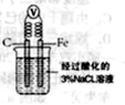
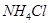 固体中混有的少量的碘
固体中混有的少量的碘