题目内容
常温下测得浓度均为0.1 mol·L—1的下列三种溶液的pH:
下列说法中错误的是
A.溶液中阳离子物质的量之和的关系为:Na2CO3>NaHCO3=NaCN
B.相同条件下的酸性:H2CO3>HCN
C.三种溶液中均存在电离平衡和水解平衡
D.升高Na2CO3溶液的温度会使c(HCO3—)/ c(CO32—)增大
| 溶 质 | NaHCO3 | Na2CO3 | NaCN |
| pH | 8.4 | 11.6 | 11.1 |
下列说法中错误的是
A.溶液中阳离子物质的量之和的关系为:Na2CO3>NaHCO3=NaCN
B.相同条件下的酸性:H2CO3>HCN
C.三种溶液中均存在电离平衡和水解平衡
D.升高Na2CO3溶液的温度会使c(HCO3—)/ c(CO32—)增大
A
试题分析:A、溶液中阳离子物质的量之和,因三种溶液的体积不确定,无法比较物质的量的大小,错误;B、根据“越弱越水解”盐的水解规律,NaCN水解程度大于NaHCO3水解程度,所以酸性:H2CO3>HCN,正确;C、都存在水的电离平衡以及相应的弱酸根离子的水解平衡,正确;D、升高温度促进Na2CO3水解,平衡正向移动,会使c(HCO3—)/ c(CO32—)增大,正确。

练习册系列答案
相关题目
 mol·L-1
mol·L-1 =1×10-8,下列叙述不正确的是( )
=1×10-8,下列叙述不正确的是( )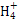 )+c(H+)=c(Cl-)+c(OH-)
)+c(H+)=c(Cl-)+c(OH-)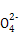 )
)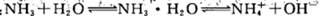 改变下列条件,能使电离程度增大的是
改变下列条件,能使电离程度增大的是 NH4+ +OH-。往其中加入少量0.01 mol·L-1NaOH溶液,保持不变的是( )
NH4+ +OH-。往其中加入少量0.01 mol·L-1NaOH溶液,保持不变的是( )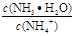 的值都变小
的值都变小