题目内容
常温下,0.1 mol/L氨水溶液中 =1×10-8,下列叙述不正确的是( )
=1×10-8,下列叙述不正确的是( )
 =1×10-8,下列叙述不正确的是( )
=1×10-8,下列叙述不正确的是( )| A.该溶液中氢离子的浓度:c(H+)=1×10-11 mol/L |
B.0.1 mol/L氨水溶液与0.1 mol/L HCl溶液等体积混合后所得溶液中:c(N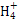 )+c(H+)=c(Cl-)+c(OH-) )+c(H+)=c(Cl-)+c(OH-) |
C.0.1 mol/L的氨水溶液与0.05 mol/L H2SO4溶液等体积混合后所得溶液中:c(N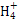 )+c(NH3)+c(NH3·H2O)=2c(S )+c(NH3)+c(NH3·H2O)=2c(S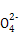 ) ) |
D.浓度均为0.1 mol/L的NH3·H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则c(N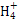 )>c(NH3·H2O)>c(Cl-)>c(OH-)>c(H+) )>c(NH3·H2O)>c(Cl-)>c(OH-)>c(H+) |
D
根据氨水中 =1×10-8,结合水的离子积,可求得c(H+)=1×10-11mol/L,A项正确;氨水和盐酸恰好反应生成氯化铵,根据电荷守恒,可得c(N
=1×10-8,结合水的离子积,可求得c(H+)=1×10-11mol/L,A项正确;氨水和盐酸恰好反应生成氯化铵,根据电荷守恒,可得c(N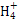 )+c(H+)=c(Cl-)+c(OH-),B项正确;氨水和硫酸恰好反应生成硫酸铵,根据物料守恒,可得c(N
)+c(H+)=c(Cl-)+c(OH-),B项正确;氨水和硫酸恰好反应生成硫酸铵,根据物料守恒,可得c(N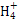 )+c(NH3)+c(NH3·H2O)=2c(S
)+c(NH3)+c(NH3·H2O)=2c(S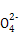 ),C项正确;由于混合后溶液显碱性,说明一水合氨的电离程度大于N
),C项正确;由于混合后溶液显碱性,说明一水合氨的电离程度大于N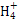 的水解程度,故c(Cl-)大于c(NH3·H2O),D项不正确。
的水解程度,故c(Cl-)大于c(NH3·H2O),D项不正确。
 =1×10-8,结合水的离子积,可求得c(H+)=1×10-11mol/L,A项正确;氨水和盐酸恰好反应生成氯化铵,根据电荷守恒,可得c(N
=1×10-8,结合水的离子积,可求得c(H+)=1×10-11mol/L,A项正确;氨水和盐酸恰好反应生成氯化铵,根据电荷守恒,可得c(N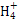 )+c(H+)=c(Cl-)+c(OH-),B项正确;氨水和硫酸恰好反应生成硫酸铵,根据物料守恒,可得c(N
)+c(H+)=c(Cl-)+c(OH-),B项正确;氨水和硫酸恰好反应生成硫酸铵,根据物料守恒,可得c(N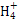 )+c(NH3)+c(NH3·H2O)=2c(S
)+c(NH3)+c(NH3·H2O)=2c(S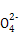 ),C项正确;由于混合后溶液显碱性,说明一水合氨的电离程度大于N
),C项正确;由于混合后溶液显碱性,说明一水合氨的电离程度大于N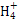 的水解程度,故c(Cl-)大于c(NH3·H2O),D项不正确。
的水解程度,故c(Cl-)大于c(NH3·H2O),D项不正确。
练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
 HClO + OHˉ的平衡常数K≈10ˉ7.6
HClO + OHˉ的平衡常数K≈10ˉ7.6
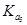 >
>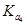 >
>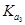
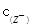 /
/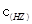 ·
·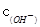 的比值变小,若加少量盐酸,则比值变大
的比值变小,若加少量盐酸,则比值变大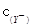 <
<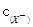
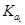 >
>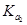 >
>