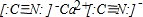题目内容
为了检验某化合物中是否含有NH4+、SO42-、Fe2+和结晶水,设计了下列操作步骤:
①取少量晶体加热,发现试管口处有液体,且该液体能使无水硫酸铜变蓝;
②另取少量晶体溶于水中,加入KSCN溶液,再滴加少量的氯水,有红色出现;
③取少量溶液于试管,加入盐酸,没有反应现象,再加入BaC12溶液,有白色沉淀生成; ④取少量溶液于试管中,加入浓NaOH溶液,微热有使湿润的红色石蕊试纸变蓝的气体产生,同时也有白色沉淀产生,该沉淀很快变成灰绿色沉淀。
下列说法不正确的是 ( )
A.②中的现象说明有Fe2+
B.通过上述实验可确定该化合物的化学式为(NH4)2Fe(SO4)2?6H2O
C.为了检测SO2-4,可以将③中的试剂换为HNO3酸化的Ba(NO3)2
D.④中的沉淀长时间放置会变红褐色沉淀
B

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目