题目内容
(2009?广东模拟)铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁.“速力菲”是市场上一种常见的补铁药物,下表格是它的说明书.

(1)该药品中Fe2+ 会缓慢氧化,国家规定该药物中Fe2+ 的氧化率超过10%即不能再服用.
1为了检验某药店出售的“速力菲”是否氧化,实验室可选用最常用最灵敏的检验试剂为
②实验室采用H2SO4酸化的KMnO4溶液,对“速力菲”中的Fe2+ 进行滴定(假设药品中,其它成分不与KMnO4反应).请配平下列离子方程式
③称量上述含铁元素质量分数为20.00% 的“速力菲”10.00g,将其全部溶于稀硫酸中,配制成1000.00mL溶液,取出20.00mL,用0.01mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL.该药品可以服用吗?
(2)已知琥珀酸亚铁相对分子质量为172,琥珀酸为有机酸.含23.6g琥珀酸的溶液与4mol/L 100mL的氢氧化钠溶液恰好完全中和.质子核磁共振分析显示,琥珀酸分子中只含有两种位置不同的氢原子.写出琥珀酸溶液与氢氧化钠溶液完全中和的离子方程式(有机物须写结构简式)

(1)该药品中Fe2+ 会缓慢氧化,国家规定该药物中Fe2+ 的氧化率超过10%即不能再服用.
1为了检验某药店出售的“速力菲”是否氧化,实验室可选用最常用最灵敏的检验试剂为
硫氰化钾溶液
硫氰化钾溶液
( 填试剂的名称 )②实验室采用H2SO4酸化的KMnO4溶液,对“速力菲”中的Fe2+ 进行滴定(假设药品中,其它成分不与KMnO4反应).请配平下列离子方程式
1
1
MnO4-+5
5
Fe2++8
8
H+═1
1
Mn2++5
5
Fe3++4
4
H2O③称量上述含铁元素质量分数为20.00% 的“速力菲”10.00g,将其全部溶于稀硫酸中,配制成1000.00mL溶液,取出20.00mL,用0.01mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL.该药品可以服用吗?
不可以
不可以
(填“可以”或“不可以”),请通过计算简述理由(写出主要计算过程)由MnO4-~5Fe2+,可得1000.00mL溶液含有的Fe2+的物质的量n(Fe2+)=0.01mol/L×12.00×10-3L×5×(1000.00mL/20.00mL)=0.03mol,m(Fe2+)=0.03mol×56g/mol=1.68g,Fe2+的氧化率(10g×20.00%-1.68g)/(10g×20.00%)=16.00%>10%,所以不可以服用.
由MnO4-~5Fe2+,可得1000.00mL溶液含有的Fe2+的物质的量n(Fe2+)=0.01mol/L×12.00×10-3L×5×(1000.00mL/20.00mL)=0.03mol,m(Fe2+)=0.03mol×56g/mol=1.68g,Fe2+的氧化率(10g×20.00%-1.68g)/(10g×20.00%)=16.00%>10%,所以不可以服用.
.(2)已知琥珀酸亚铁相对分子质量为172,琥珀酸为有机酸.含23.6g琥珀酸的溶液与4mol/L 100mL的氢氧化钠溶液恰好完全中和.质子核磁共振分析显示,琥珀酸分子中只含有两种位置不同的氢原子.写出琥珀酸溶液与氢氧化钠溶液完全中和的离子方程式(有机物须写结构简式)
HOOC-CH2-CH2-COOH+2OH-→-OOC-CH2-CH2-COO-+2H2O
HOOC-CH2-CH2-COOH+2OH-→-OOC-CH2-CH2-COO-+2H2O
,琥珀酸亚铁的化学式为FeC4H4O4
FeC4H4O4
.分析:(1)根据Fe2+氧化会生成成Fe3+,即检验Fe3+的存在;
②根据化合价升降总数相等和质量守恒来配平;
③根据关系式:MnO4-~5Fe2+,利用KMnO4的物质的量来求出1000.00mL溶液含有的Fe2+的物质的量,然后求出Fe2+ 的氧化率来解答;
(2)采用讨论法,当琥珀酸为一元酸时,根据与碱反应的关系,可得其相对分子质量为23.60.4=59,不符合有机物组成原则,当琥珀酸为二元酸时,其相对分子质量为23.60.2=118,符合题意,再根据琥珀酸分子中有两种位置不同的氢原子来解题.采用讨论法,当琥珀酸为一元酸时,根据与碱反应的关系,可得其相对分子质量为23.60.4=59,不符合有机物组成原则,当琥珀酸为二元酸时,其相对分子质量为23.60.2=118,符合题意,再根据琥珀酸分子中有两种位置不同的氢原子来解题.
②根据化合价升降总数相等和质量守恒来配平;
③根据关系式:MnO4-~5Fe2+,利用KMnO4的物质的量来求出1000.00mL溶液含有的Fe2+的物质的量,然后求出Fe2+ 的氧化率来解答;
(2)采用讨论法,当琥珀酸为一元酸时,根据与碱反应的关系,可得其相对分子质量为23.60.4=59,不符合有机物组成原则,当琥珀酸为二元酸时,其相对分子质量为23.60.2=118,符合题意,再根据琥珀酸分子中有两种位置不同的氢原子来解题.采用讨论法,当琥珀酸为一元酸时,根据与碱反应的关系,可得其相对分子质量为23.60.4=59,不符合有机物组成原则,当琥珀酸为二元酸时,其相对分子质量为23.60.2=118,符合题意,再根据琥珀酸分子中有两种位置不同的氢原子来解题.
解答:解:(1)①Fe2+氧化会生成成Fe3+,可用硫氰化钾溶液检验Fe3+的存在,故答案为:硫氰化钾溶液;
②MnO4-中Mn的化合价由+7价降为+2价,变化5,Fe2+中Fe由+2价升为+3价,变化1,根据化合价升降总数相等和质量守恒得:1MnO4-+5Fe2++8H+═1Mn2++5Fe3++4H2O,
故答案为:1;5;8;1;5;4;
③由MnO4-~5Fe2+,可得1000.00mL溶液含有的Fe2+的物质的量n(Fe2+)=0.01 mol/L×12.00×10-3L×5×(1000.00 mL/20.00 mL)=0.03 mol,m(Fe2+)=0.03 mol×56 g/mol=1.68 g,Fe2+的氧化率(10 g×20.00%-1.68 g)/(10 g×20.00%)=16.00%>10%,所以不可以服用,
故答案为:不可以;由MnO4-~5Fe2+,可得1000.00mL溶液含有的Fe2+的物质的量n(Fe2+)=0.01 mol/L×12.00×10-3L×5×(1000.00 mL/20.00 mL)=0.03 mol,m(Fe2+)=0.03 mol×56 g/mol=1.68 g,Fe2+的氧化率(10 g×20.00%-1.68 g)/(10 g×20.00%)=16.00%>10%,所以不可以服用;
(2)当琥珀酸为一元酸时,根据与碱反应的关系,其相对分子质量为23.60.4=59,不符合有机物组成原则,当琥珀酸为二元酸时,其相对分子质量为23.60.2=118,又琥珀酸分子中有两种位置不同的氢原子,所以琥珀酸的结构等式为HOOC-CH2-CH2-COOH,琥珀酸溶液与氢氧化钠溶液完全中和的离子方程式:HOOC-CH2-CH2-COOH+2OH-→-OOC-CH2-CH2-COO-+2H2O,琥珀酸亚铁的化学式为FeC4H4O4,故答案为:HOOC-CH2-CH2-COOH+2OH-→-OOC-CH2-CH2-COO-+2H2O;FeC4H4O4.
②MnO4-中Mn的化合价由+7价降为+2价,变化5,Fe2+中Fe由+2价升为+3价,变化1,根据化合价升降总数相等和质量守恒得:1MnO4-+5Fe2++8H+═1Mn2++5Fe3++4H2O,
故答案为:1;5;8;1;5;4;
③由MnO4-~5Fe2+,可得1000.00mL溶液含有的Fe2+的物质的量n(Fe2+)=0.01 mol/L×12.00×10-3L×5×(1000.00 mL/20.00 mL)=0.03 mol,m(Fe2+)=0.03 mol×56 g/mol=1.68 g,Fe2+的氧化率(10 g×20.00%-1.68 g)/(10 g×20.00%)=16.00%>10%,所以不可以服用,
故答案为:不可以;由MnO4-~5Fe2+,可得1000.00mL溶液含有的Fe2+的物质的量n(Fe2+)=0.01 mol/L×12.00×10-3L×5×(1000.00 mL/20.00 mL)=0.03 mol,m(Fe2+)=0.03 mol×56 g/mol=1.68 g,Fe2+的氧化率(10 g×20.00%-1.68 g)/(10 g×20.00%)=16.00%>10%,所以不可以服用;
(2)当琥珀酸为一元酸时,根据与碱反应的关系,其相对分子质量为23.60.4=59,不符合有机物组成原则,当琥珀酸为二元酸时,其相对分子质量为23.60.2=118,又琥珀酸分子中有两种位置不同的氢原子,所以琥珀酸的结构等式为HOOC-CH2-CH2-COOH,琥珀酸溶液与氢氧化钠溶液完全中和的离子方程式:HOOC-CH2-CH2-COOH+2OH-→-OOC-CH2-CH2-COO-+2H2O,琥珀酸亚铁的化学式为FeC4H4O4,故答案为:HOOC-CH2-CH2-COOH+2OH-→-OOC-CH2-CH2-COO-+2H2O;FeC4H4O4.
点评:本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力,增加了学生分析问题的能力,强调了学生整合知识的能力.

练习册系列答案
相关题目

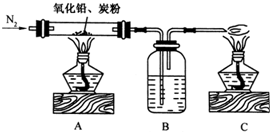 (2009?广东模拟)某课外小组欲通过实验证明方铅矿分解所得白色粉末中含有氧元素,设计以下的实验装置:
(2009?广东模拟)某课外小组欲通过实验证明方铅矿分解所得白色粉末中含有氧元素,设计以下的实验装置: