题目内容
如图在试管甲中先加入2mL 95%的乙醇, 并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验。试回答:
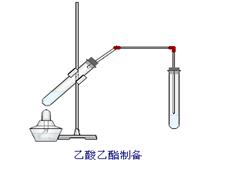
(1)试管甲中加入浓硫酸的目的是
(2)该实验中长导管的作用是 ,其不宜伸入试管乙的溶液中,原因是
(3)试管乙中饱和Na2CO3的作用是
(4)试管乙中观察到的现象是
(5)液体混合加热时液体容积不能超过其容积的 ,本实验反应开始时用小火加热的原因是 ;(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
(6)写出试管甲中发生反应的化学方程式 。

(1)试管甲中加入浓硫酸的目的是
(2)该实验中长导管的作用是 ,其不宜伸入试管乙的溶液中,原因是
(3)试管乙中饱和Na2CO3的作用是
(4)试管乙中观察到的现象是
(5)液体混合加热时液体容积不能超过其容积的 ,本实验反应开始时用小火加热的原因是 ;(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
(6)写出试管甲中发生反应的化学方程式 。
(1)催化剂、吸水剂 (2分)(2)导气、冷凝,防止加热不充分而倒吸 (3分)
(3)除去乙酸乙酯中的乙醇和乙酸,降低乙酸乙酯的溶解度,便于分层析(3分)
(4)液体分层 (1分)
(5)1/3;加快反应速率,同时又防止了反应物未来得及反应而挥发损失(3分)
(6)H2SO4+2CH3COONa +2CH3CH2OH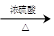 2CH3COOC2H5 +2H2O+Na2SO4 (3分)
2CH3COOC2H5 +2H2O+Na2SO4 (3分)
(3)除去乙酸乙酯中的乙醇和乙酸,降低乙酸乙酯的溶解度,便于分层析(3分)
(4)液体分层 (1分)
(5)1/3;加快反应速率,同时又防止了反应物未来得及反应而挥发损失(3分)
(6)H2SO4+2CH3COONa +2CH3CH2OH
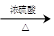 2CH3COOC2H5 +2H2O+Na2SO4 (3分)
2CH3COOC2H5 +2H2O+Na2SO4 (3分)试题分析:(1)由于酯化反应是可逆反应,则试管中加入浓硫酸的目的是起到催化剂和吸水剂的作用。
(2)由于生成的乙酸乙酯、乙醇和乙酸都是易挥发的,所以长导管的作用是导气,同时兼起冷凝回流作用。由于乙醇和乙酸都是和水互溶的,因此导管不宜伸入试管溶液中的原因是防止加热不充分而倒吸。
(3)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,目的是除去乙醇和乙酸、便于闻乙酸乙酯的香味,降低乙酸乙酯的溶解度,便于分层。
(4)乙酸乙酯不溶于水,所以试管乙中观察到的现象是液体分层。
(5)液体混合加热时液体容积不能超过其容积的1/3。根据有关物质的沸点可知,本实验反应开始时用小火加热的原因是一方面加快反应速率,另一方面又防止了反应物未来得及反应而挥发损失。
(6)由于醋酸钠和浓硫酸反应生成醋酸,进而醋酸和乙醇发生酯化反应,所以试管甲中发生反应的化学方程式是H2SO4+2CH3COONa +2CH3CH2OH
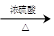 2CH3COOC2H5 +2H2O+Na2SO4。
2CH3COOC2H5 +2H2O+Na2SO4。点评:该题紧扣教材,基础性强,有利于调动学生的学习兴趣,激发学生的学习积极性。该题是基础性实验题的考查,旨在培养学生规范严谨的实验设计能力,有利于提高学生的应试能力和学习效率。

练习册系列答案
相关题目