题目内容
实验室中制备HClO溶液的最好方法是将Cl2缓慢通入( )
| A、蒸馏水 | B、烧碱溶液 |
| C、纯碱溶液 | D、石灰石的悬浊液 |
考点:氯气的化学性质
专题:卤族元素
分析:氯气与水反应为可逆反应,且生成盐酸,HClO与烧碱、纯碱反应,不能制备HClO,结合平衡移动分析.
解答:
解:A.氯气与水反应为可逆反应,且生成盐酸,产物不纯,故A不选;
B.与烧碱反应,不能制备HClO,故B不选;
C.与纯碱反应,不能制备HClO,故C不选;
D.由Cl2+H2O?HCl+HClO可知,石灰石的悬浊液可与HCl反应,平衡正向移动,则实验室中制备HClO溶液的最好方法是将Cl2缓慢通入石灰石的悬浊液,故D选;
故选D.
B.与烧碱反应,不能制备HClO,故B不选;
C.与纯碱反应,不能制备HClO,故C不选;
D.由Cl2+H2O?HCl+HClO可知,石灰石的悬浊液可与HCl反应,平衡正向移动,则实验室中制备HClO溶液的最好方法是将Cl2缓慢通入石灰石的悬浊液,故D选;
故选D.
点评:本题考查氯气的性质及HClO的制备,为高频考点,把握制备原理及平衡移动为解答的关键,注意制备HClO不能混有杂质,HClO不能发生反应,题目难度不大.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
如图所示的实验操作,能达到相应目的是( )
A、 干燥Cl2 |
B、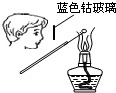 检验Na2CO3中Na+ |
C、 证明氨气极易溶于水 |
D、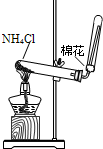 实验室制氨气 |
甲苯被式量为43的烃基取代一个氢原子后,可能得到的物质有多少种( )
| A、8种 | B、6种 | C、9种 | D、12种 |
下列化学用语正确的是( )
A、聚丙烯的结构简式为: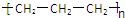 |
B、丙烷分子的比例模型为: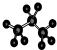 |
| C、甲醛的结构简式:HCHO |
D、羟基的电子式: |
下列物质,不能用作漂白剂的是( )
| A、SO2 |
| B、Ca(ClO)2 |
| C、H2O2 |
| D、HNO3 |
下列关于元素周期律的叙述正确的是( )
| A、随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 |
| B、元素性质的周期性变化是指原子核外电子排布、原子半径及元素主要化合价的周期性变化 |
| C、随着元素原子序数的递增,原子半径从小到大(稀有气体除外)发生周期性变化 |
| D、在元素周期表中有些元素既表现出一定的金属性又表现出一定的非金属性 |
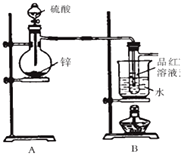 已知实验室制取氯气是用二氧化锰和浓盐酸反应的原理,在收集时,若是用排水法,可能会损失部分氯气.
已知实验室制取氯气是用二氧化锰和浓盐酸反应的原理,在收集时,若是用排水法,可能会损失部分氯气.